- 제약·바이오
- 국내사
비급여 빔팻정, 후속 제네릭은 급여등재 호시탐탐
라코사미드 복제약 경쟁…급여로 시장 경쟁 우위 전략

최선 기자
기사입력: 2016-11-18 05:00:53
-
가
지난 8월 재심사(PMS) 만료로 차세대 간질치료제 빔팻정(성분명 라코사미드) 제네릭 경쟁이 불붙고 있다.
오리지널 빔팻정이 비급여인 까닭에 후발 주자들은 급여를 신청해 시장 경쟁에서 우위를 점하겠다는 계획이다.
17일 식품의약품안전처에 따르면 환인제약은 라코사미드 제네릭 네오팻정 50mg과 100mg 두 품목을 승인받았다.
라코사미드는 16세 이상의 간질 환자에서 2차성 전신발작을 동반하거나 동반하지 않는 부분발작 치료의 부가요법으로 쓰이는 치료제.
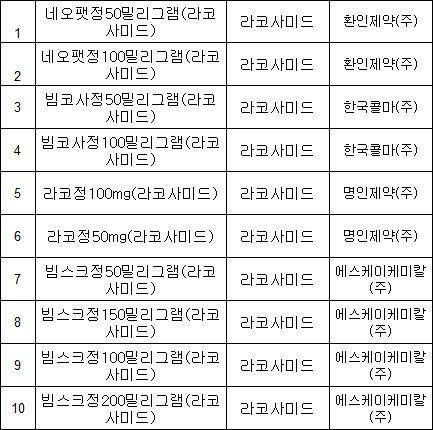
식품의약품안전처, 라코사미드 제네릭 품목 허가 사항
지난 8월 SK케미칼의 빔스크정 첫 허가를 필두로 명인제약의 라코정, 한국콜마의 빔코사정이 허가를 받은데 이어 최근 환인제약까지 가세했다.
한국유씨비제약은 오리지널 빔팻정을 2010년 8월 품목 허가를 받은 후 2011년 12월 시장에 정식 출시한 바 있다.
빔팻정은 50mg, 100mg, 150mg, 200mg 네 가지 라인업을 갖추고 있지만 시장 출시 용량은 50mg, 100mg 두 품목뿐이었다.
환인제약과 한국콜마 빔코사정, 명인제약 라코정 역시 오리지널 50mg, 100mg 두 용량으로만 허가를 받았다.
제네릭 1호 SK케미칼 빔스크정은 빔팻정과 동일하게 네 가지 용량을 모두 허가 받아 처방시 선택의 폭이라는 강점을 가졌다.
흥미로운 점은 후발 주자들의 급여 등재 신청.
SK케미칼뿐 아니라 명인제약, 환인제약도 건강보험심사평가원에 급여를 신청했거나 예정 중에 있어 비급여 빔팻정과의 경쟁에서 우위를 점한다는 계획이다.
SK케미칼 관계자는 "빔스크정의 급여를 추진하고 있어 급여등재시 비급여 빔팻정 대비 시장 경쟁에 유리할 것으로 보인다"며 "4가지 용량으로 허가받은 것 역시 처방 옵션이 늘어난 것이기 때문에 긍정적이다"고 덧붙였다.
환인제약 관계자는 "전문약이다 보니 급여가 되지 않으면 매출 증진을 기대하기 어렵다"며 "그런 까닭에 급여를 신청할 예정이지만 오리지널 약가라는 기준이 없다보니 약가 협상에서 각 제약사간 눈치 싸움이 치열하지 않을까 한다"고 덧붙였다.
오리지널 빔팻정이 비급여인 까닭에 후발 주자들은 급여를 신청해 시장 경쟁에서 우위를 점하겠다는 계획이다.
17일 식품의약품안전처에 따르면 환인제약은 라코사미드 제네릭 네오팻정 50mg과 100mg 두 품목을 승인받았다.
라코사미드는 16세 이상의 간질 환자에서 2차성 전신발작을 동반하거나 동반하지 않는 부분발작 치료의 부가요법으로 쓰이는 치료제.

한국유씨비제약은 오리지널 빔팻정을 2010년 8월 품목 허가를 받은 후 2011년 12월 시장에 정식 출시한 바 있다.
빔팻정은 50mg, 100mg, 150mg, 200mg 네 가지 라인업을 갖추고 있지만 시장 출시 용량은 50mg, 100mg 두 품목뿐이었다.
환인제약과 한국콜마 빔코사정, 명인제약 라코정 역시 오리지널 50mg, 100mg 두 용량으로만 허가를 받았다.
제네릭 1호 SK케미칼 빔스크정은 빔팻정과 동일하게 네 가지 용량을 모두 허가 받아 처방시 선택의 폭이라는 강점을 가졌다.
흥미로운 점은 후발 주자들의 급여 등재 신청.
SK케미칼뿐 아니라 명인제약, 환인제약도 건강보험심사평가원에 급여를 신청했거나 예정 중에 있어 비급여 빔팻정과의 경쟁에서 우위를 점한다는 계획이다.
SK케미칼 관계자는 "빔스크정의 급여를 추진하고 있어 급여등재시 비급여 빔팻정 대비 시장 경쟁에 유리할 것으로 보인다"며 "4가지 용량으로 허가받은 것 역시 처방 옵션이 늘어난 것이기 때문에 긍정적이다"고 덧붙였다.
환인제약 관계자는 "전문약이다 보니 급여가 되지 않으면 매출 증진을 기대하기 어렵다"며 "그런 까닭에 급여를 신청할 예정이지만 오리지널 약가라는 기준이 없다보니 약가 협상에서 각 제약사간 눈치 싸움이 치열하지 않을까 한다"고 덧붙였다.

관련기사
- "제네릭 비켜!" 특허 만료에도 적수없는 리바로 2016-11-01 05:00:53
- "타미플루 아성에 도전" 독감 치료제 후발 주자는? 2016-10-12 12:00:36
- 타세바 특허만료 코 앞…폐암 제네릭 시장 '후끈' 2016-10-11 05:00:11









