- 제약·바이오
- 국내사
바이넥스 이어 비보존도 9개 품목 제조·판매 중지
발행날짜: 2021-03-12 12:00:46
-
가
-
식약처, 의약품 위수탁 제조소 긴급 특별 점검
사전·예방적 차원 조치…해당 제품 처방 제한
바이넥스에 이어 비보존도 허가사항과 다르게 의약품을 제조한 사유로 9개 품목의 제조, 판매가 중지된다.
12일 식품의약품안전처는 정기점검 시 비보존제약에서 허가 또는 신고된 사항과 다르게 의약품을 제조(수탁제조 포함)한 것을 확인해 조치했다고 밝혔다.
이번 조치는 비보존제약이 자사에서 제조한 판매용 4개 의약품과 타사로부터 위탁받아 수탁 제조한 5개 의약품을 허가사항과 다르게 제조한 것을 확인한 데 따른 것으로 식약처는 해당 품목을 잠정 제조·판매중지 및 회수 조치하기로 했고 이는 사전·예방적 차원의 조치이다.
대상 품목은 ▲비보존제약의 디스트린캡슐(디아세레인), 레디씬캡슐, 뮤코리드캅셀200mg(아세틸시스테인), 제이옥틴정(티옥트산) ▲뉴젠팜 디아젠캡슐 ▲휴비스트제약 아트로세린캡슐 ▲넥스팜코리아 뮤코반캡슐200mg ▲다산제약 뮤코티아캡슐200mg ▲메딕스제약 티옥신정(티옥트산)까지 9개다.
식약처는 의‧약사 등 전문가에게 해당 제품을 다른 대체 의약품으로 전환하고 제품 회수가 적절히 수행될 수 있도록 협조 요청하는 안전성 속보를 의‧약사 및 소비자 등에게 배포하는 한편 보건복지부 및 건강보험심사평가원을 통해 병·의원 등에 해당 제품에 대한 처방 제한을 요청했다.
연이어 허가 위반 사항이 적발됨에 따라 식약처는 전국의 위‧수탁 제조소 30개소에 대해 긴급 특별 점검을 실시한다.
식약처는 점검 결과 등을 고려해 향후 의약품 제조소 전체에 대한 점검으로 확대하는 등 재발방지를 위한 종합적 제도개선 방안도 신속하게 마련해 추진할 계획이다.
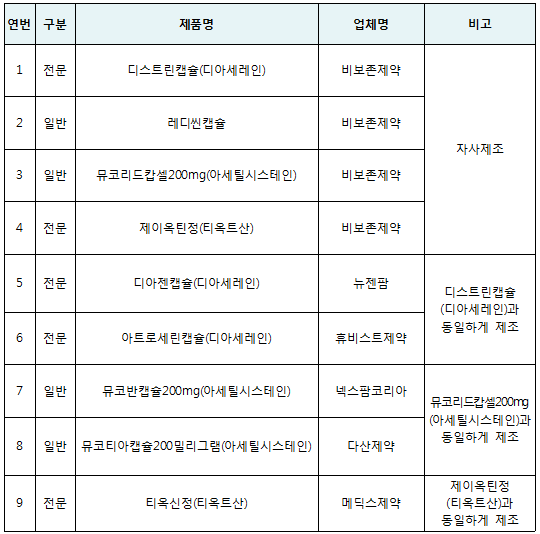
대상 의약품 (6개사 9개 품목)
12일 식품의약품안전처는 정기점검 시 비보존제약에서 허가 또는 신고된 사항과 다르게 의약품을 제조(수탁제조 포함)한 것을 확인해 조치했다고 밝혔다.
이번 조치는 비보존제약이 자사에서 제조한 판매용 4개 의약품과 타사로부터 위탁받아 수탁 제조한 5개 의약품을 허가사항과 다르게 제조한 것을 확인한 데 따른 것으로 식약처는 해당 품목을 잠정 제조·판매중지 및 회수 조치하기로 했고 이는 사전·예방적 차원의 조치이다.
대상 품목은 ▲비보존제약의 디스트린캡슐(디아세레인), 레디씬캡슐, 뮤코리드캅셀200mg(아세틸시스테인), 제이옥틴정(티옥트산) ▲뉴젠팜 디아젠캡슐 ▲휴비스트제약 아트로세린캡슐 ▲넥스팜코리아 뮤코반캡슐200mg ▲다산제약 뮤코티아캡슐200mg ▲메딕스제약 티옥신정(티옥트산)까지 9개다.
식약처는 의‧약사 등 전문가에게 해당 제품을 다른 대체 의약품으로 전환하고 제품 회수가 적절히 수행될 수 있도록 협조 요청하는 안전성 속보를 의‧약사 및 소비자 등에게 배포하는 한편 보건복지부 및 건강보험심사평가원을 통해 병·의원 등에 해당 제품에 대한 처방 제한을 요청했다.
연이어 허가 위반 사항이 적발됨에 따라 식약처는 전국의 위‧수탁 제조소 30개소에 대해 긴급 특별 점검을 실시한다.
식약처는 점검 결과 등을 고려해 향후 의약품 제조소 전체에 대한 점검으로 확대하는 등 재발방지를 위한 종합적 제도개선 방안도 신속하게 마련해 추진할 계획이다.
관련기사
- '바이넥스 사태' 고개 숙인 제약업계…CMO 사업 찬물 2021-03-11 10:42:11
- 바이넥스 사태 일파만파...위탁생산 제재로 국내사 불똥 2021-03-10 05:45:57
- 바이넥스 수탁 품목도 판매 중지…24개사 32품목 대상 2021-03-09 15:11:28
- 바이넥스 판매 중지 처분 파장…처방 시장 영향은 미비 2021-03-09 05:45:45






