- 정책
- 제도・법률
심평원, 키트루다·옵디보 '허가초과' 신속 승인
발행날짜: 2017-09-19 17:23:14
-
가
-
위암 등 6개 암종에 허가초과 사용 승인
면역관문억제제인 키트루다와 옵디보의의 허가외 사용(이하 허가초과) 승인이 6개 암종에 승인이 났다.
건강보험심사평가원은 19일 요양기관에서 다학제적위원회의 협의를 거쳐 신청한 키트루다주(성분명: pembrolizumab), 옵디보주(성분명: nivolumab)의 허가초과에 대해 암질환심의위원회의 심의를 거쳐 승인을 결정했다고 밝혔다.
이는 심평원 이병일 약제관리실장이 최근 해당 환자들과 간담회에서 신속 검토하기로 했던 약속을 지키기 위함이다.
당초 10월 중순 경 개최 예정이었던 암질환심의위원회 회의를 앞당겨 9월 18일에 개최해 결정된 데 따른 것이다.
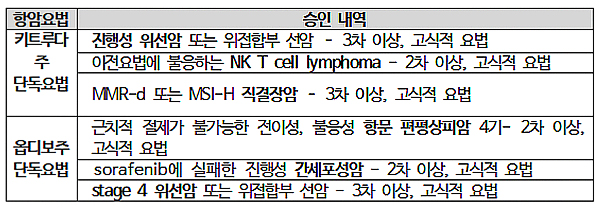
이번 논의 주요사항은 ▲옵디보 단독요법에 위암, 간세포암, 항문암 등 3개 요법 ▲ 키트루다 단독요법에 위암, 비호지킨림프종, 직결장암등 3개 요법이 승인됐다.
사전신청 해당 요양기관은 암질환심의위원회가 승인한 요법에 대해서 사용승인 통보를 받은 날부터 허가초과로 환자에게 투약할 수 있고, 약값은 환자가 전액 본인 부담한다.
승인된 요법에 대해서는 타 요양기관에서도 사용승인 신청서를 내면 간단한 행정절차만 거쳐 신속히 승인이 이뤄지기 때문에, 면역관문억제제를 허가초과로 사용하고자 하는 환자들은 빠른 처방을 받을 수 있게 됐다.
심평원 이병일 약제관리실장은 "사전신청 되는 허가초과 면역관문억제제는 신속한 승인이 이루어질 수 있도록 하겠다"고 밝혔다.
한편, 이번에 사전신청으로 승인된 항암요법에 대한 상세한 내용은 심평원 홈페이지→의료정보→의약품정보→암질환사용 약제 및 요법→항암화학요법→사전신청요법에서 확인할 수 있다.
건강보험심사평가원은 19일 요양기관에서 다학제적위원회의 협의를 거쳐 신청한 키트루다주(성분명: pembrolizumab), 옵디보주(성분명: nivolumab)의 허가초과에 대해 암질환심의위원회의 심의를 거쳐 승인을 결정했다고 밝혔다.
이는 심평원 이병일 약제관리실장이 최근 해당 환자들과 간담회에서 신속 검토하기로 했던 약속을 지키기 위함이다.

이번 논의 주요사항은 ▲옵디보 단독요법에 위암, 간세포암, 항문암 등 3개 요법 ▲ 키트루다 단독요법에 위암, 비호지킨림프종, 직결장암등 3개 요법이 승인됐다.
사전신청 해당 요양기관은 암질환심의위원회가 승인한 요법에 대해서 사용승인 통보를 받은 날부터 허가초과로 환자에게 투약할 수 있고, 약값은 환자가 전액 본인 부담한다.
승인된 요법에 대해서는 타 요양기관에서도 사용승인 신청서를 내면 간단한 행정절차만 거쳐 신속히 승인이 이뤄지기 때문에, 면역관문억제제를 허가초과로 사용하고자 하는 환자들은 빠른 처방을 받을 수 있게 됐다.
심평원 이병일 약제관리실장은 "사전신청 되는 허가초과 면역관문억제제는 신속한 승인이 이루어질 수 있도록 하겠다"고 밝혔다.
한편, 이번에 사전신청으로 승인된 항암요법에 대한 상세한 내용은 심평원 홈페이지→의료정보→의약품정보→암질환사용 약제 및 요법→항암화학요법→사전신청요법에서 확인할 수 있다.
관련기사
- "면역항암제, 다학제진료 가능 병원 처방이 관건" 2017-09-13 16:39:02
- 폐암 면역항암제 2종 승부처 "동반진단법에 주목" 2017-09-13 05:00:33






