- 제약·바이오
- 국내사
계륵 전락한 콜린알포세레이트…잇따라 판매정지 처분
발행날짜: 2021-01-26 05:45:55
-
가
-
최근 일주일새 총 12개 업체 2개월 행정처분 철퇴
중소 제약사, 품목 유지-취하 따른 실익 두고 저울질
중소 제약사를 중심으로 콜린알포세레이트에 대한 고심이 깊어지고 있다.
종근당, 대웅바이오로 재편된 철옹성을 뚫기 힘들뿐더러 품목 유지를 위해 들어가는 임상 비용도 만만치 않기 때문이다.
특히 일부 제약사들은 품목 취하를 자진 선택했지만 일부는 끝까지 품목 유지 여부를 결정하지 못한채 임상 재평가 계획서 제출 시한을 넘기면서 판매정지 처분이 불가피지는 상황까지 몰리고 있다.
25일 식품의약품안전처에 따르면 이달 12일부터 18일까지 총 12개의 회사가 콜린알포세레이트 임상 재평가 계획서 미제출로 해당 품목 판매업무정지 2개월 처분을 받은 것으로 확인됐다.
해당 업체는 알피바이오, 케이엠에스제약, 인트로바이오파마, 새한제약, 한국피엠지제약, 오스틴제약, 미래제약, 삼익제약, 다나젠, 아이큐어, 케이에스제약, 신텍스제약이다.
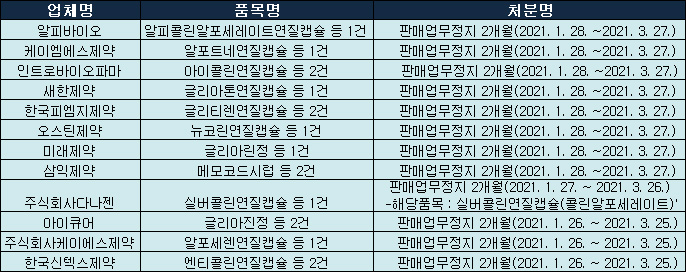
콜린알포세레이트 판매정지 처분 업체 목록
뇌기능개선제 콜린알포세레이트는 ▲뇌혈관 결손에 의한 2차 증상 및 변성 또는 퇴행성 뇌기질성 정신증후군 : 기억력저하와 착란, 의욕 및 자발성저하로 인한 방향감각장애, 의욕 및 자발성저하, 집중력 감소 ▲감정 및 행동변화 : 정서불안, 자극과민성, 주위무관심 ▲노인성 가성우울증을 적응증으로 허가됐다.
식약처는 콜린알포세레이트와 관련 효능 논란이 지속적으로 불거지자 작년 12월 23일까지 임상 재평가 계획서를 제출토록 했다. 계획서 제출이 없으면 24일 이후 판매 업무 정지 처분을 시작으로 최종 품목 허가 취소까지 진행한다는 방침.
대웅바이오·종근당은 컨소시엄을 구성, 약 300억원에 달하는 임상 재평가를 진행하기 위해 여러 업체들을 규합하고 있지만 중소형 제약사들은 비용 부담을 이유로 품목 유지 대신 품목 철회 카드를 꺼내들었다.
작년부터 이달 18일까지 콜린알포세레이트 품목 취하 수는 101개에 달한다. 이중 임상 재평가 계획서 제출 마감일인 23일에만 총 28개 업체가 품목 취하를 신청할 정도로 품목 유지/취하의 실익을 두고 제약사들의 고심이 깊었던 것으로 알려졌다.
자진 품목 취하를 선택하면 재고 물량에 대해 판매 유예기간이 주어진다. 그럼에도 불구하고 알피바이오, 케이엠에스제약 등 12개 제약사들은 임상 재평가 계획서 미제출뿐 아니라 자진 품목 취하 신청도 없어 행정처분으로 가닥이 잡혔다. 왜 이런 선택을 했을까.
업계 관계자는 "콜린알포세레이트 시장이 대웅바이오와 종근당 양강체제로 구축돼있어 중소형 업체들이 비집고 들어가기 힘든데다 정치권에서 환수 이야기가 나오는 것도 부담이었다"며 "이에 연 매출이 억 단위에 그치는 회사들은 품목 유지 대신 자진 취소를 결정했다"고 말했다.
그는 "임상 계획서를 미제출한 업체들은 끝까지 품목 유지냐 취소냐 여부를 두고 결정을 못내린 것으로 안다"며 "일단 실제 임상이 들어가기까지 시일이 남았다는 점에서 당분간 관망하는 자세를 유지할 것으로 보인다"고 밝혔다.
임상 재평가에는 약 300억원 가량이 소요되기 때문에 컨소시엄에 참여하는 업체 수에 따라 각자 분담해야 하는 비용이 달라진다.
컨소시엄 참여 업체 수가 불확실하던 12월 당시, 제약사 입장에선 성급히 임상 참여나 품목 취하를 결정하기 보다는 당장 품목판매정지 처분을 받더라도 관망모드를 유지하는게 실익이라고 판단했다는 뜻.
실제로 이번에 행정처분을 받은 업체는 자본이 충분치 않은 중소형 제약사에 국한된다.
식약처 관계자는 "현재까지의 행정처분에 이어 다음주부터 각 지방청마다 행정처분이 추가된다"며 "의견조회 기간 등이 상이해서 업체별 처분 일자가 달라졌다"고 말했다.
그는 "2개월의 판매업무 중지 처분을 시작으로, 이후에도 제출하지 않으면 6개월 판매 중지를 거쳐 최종 품목 허가 취소를 한다"며 "따라서 업체가 임상을 할지, 품목 취하를 할지 적절한 판단은 그 기간 안에 나올 것으로 본다"고 덧붙였다.
종근당, 대웅바이오로 재편된 철옹성을 뚫기 힘들뿐더러 품목 유지를 위해 들어가는 임상 비용도 만만치 않기 때문이다.
특히 일부 제약사들은 품목 취하를 자진 선택했지만 일부는 끝까지 품목 유지 여부를 결정하지 못한채 임상 재평가 계획서 제출 시한을 넘기면서 판매정지 처분이 불가피지는 상황까지 몰리고 있다.
25일 식품의약품안전처에 따르면 이달 12일부터 18일까지 총 12개의 회사가 콜린알포세레이트 임상 재평가 계획서 미제출로 해당 품목 판매업무정지 2개월 처분을 받은 것으로 확인됐다.
해당 업체는 알피바이오, 케이엠에스제약, 인트로바이오파마, 새한제약, 한국피엠지제약, 오스틴제약, 미래제약, 삼익제약, 다나젠, 아이큐어, 케이에스제약, 신텍스제약이다.

식약처는 콜린알포세레이트와 관련 효능 논란이 지속적으로 불거지자 작년 12월 23일까지 임상 재평가 계획서를 제출토록 했다. 계획서 제출이 없으면 24일 이후 판매 업무 정지 처분을 시작으로 최종 품목 허가 취소까지 진행한다는 방침.
대웅바이오·종근당은 컨소시엄을 구성, 약 300억원에 달하는 임상 재평가를 진행하기 위해 여러 업체들을 규합하고 있지만 중소형 제약사들은 비용 부담을 이유로 품목 유지 대신 품목 철회 카드를 꺼내들었다.
작년부터 이달 18일까지 콜린알포세레이트 품목 취하 수는 101개에 달한다. 이중 임상 재평가 계획서 제출 마감일인 23일에만 총 28개 업체가 품목 취하를 신청할 정도로 품목 유지/취하의 실익을 두고 제약사들의 고심이 깊었던 것으로 알려졌다.
자진 품목 취하를 선택하면 재고 물량에 대해 판매 유예기간이 주어진다. 그럼에도 불구하고 알피바이오, 케이엠에스제약 등 12개 제약사들은 임상 재평가 계획서 미제출뿐 아니라 자진 품목 취하 신청도 없어 행정처분으로 가닥이 잡혔다. 왜 이런 선택을 했을까.
업계 관계자는 "콜린알포세레이트 시장이 대웅바이오와 종근당 양강체제로 구축돼있어 중소형 업체들이 비집고 들어가기 힘든데다 정치권에서 환수 이야기가 나오는 것도 부담이었다"며 "이에 연 매출이 억 단위에 그치는 회사들은 품목 유지 대신 자진 취소를 결정했다"고 말했다.
그는 "임상 계획서를 미제출한 업체들은 끝까지 품목 유지냐 취소냐 여부를 두고 결정을 못내린 것으로 안다"며 "일단 실제 임상이 들어가기까지 시일이 남았다는 점에서 당분간 관망하는 자세를 유지할 것으로 보인다"고 밝혔다.
임상 재평가에는 약 300억원 가량이 소요되기 때문에 컨소시엄에 참여하는 업체 수에 따라 각자 분담해야 하는 비용이 달라진다.
컨소시엄 참여 업체 수가 불확실하던 12월 당시, 제약사 입장에선 성급히 임상 참여나 품목 취하를 결정하기 보다는 당장 품목판매정지 처분을 받더라도 관망모드를 유지하는게 실익이라고 판단했다는 뜻.
실제로 이번에 행정처분을 받은 업체는 자본이 충분치 않은 중소형 제약사에 국한된다.
식약처 관계자는 "현재까지의 행정처분에 이어 다음주부터 각 지방청마다 행정처분이 추가된다"며 "의견조회 기간 등이 상이해서 업체별 처분 일자가 달라졌다"고 말했다.
그는 "2개월의 판매업무 중지 처분을 시작으로, 이후에도 제출하지 않으면 6개월 판매 중지를 거쳐 최종 품목 허가 취소를 한다"며 "따라서 업체가 임상을 할지, 품목 취하를 할지 적절한 판단은 그 기간 안에 나올 것으로 본다"고 덧붙였다.
관련기사
- 재평가 테이블 오른 정맥순환제…제2 콜린알포 되나 2021-01-07 05:45:55
- 대박인줄 알았던 콜린 제형 변경…자진 취하 러시 원인은? 2020-12-14 05:45:56
- 제2의 콜린알포 선정 임박... 약가재평가 품목 12월 공개 2020-11-19 05:45:57
- 재평가후 콜린 허가사항 천차만별…처방 대란 오나 2020-11-11 05:45:50






