- 정책
- 제도・법률
당뇨병약 변경시 '투여소견' 첨부…7월 시행
복지부, 고시개정…약제투여 기준 혈당수치 등 반영

이창진 기자
기사입력: 2011-06-01 11:26:05
-
가
당뇨병치료제 단독요법 투여기준 변경시 투여소견을 첨부해야 한다.

보건복지부는 지난달 31일 이같은 내용을 골자로 한 ‘요양급여의 적용기준 및 방법에 관한 세부사항’(약제)을 고시 개정했다. 이번 고시는 7월 1일부터 시행된다.
앞서 복지부는 지난 3월말 약제 고시 개정안을 통해 메트포민 단독투여를 원칙으로 당화혈색소 기준만을 적용하고 약제 변경시 의사소견서를 첨부하도록 규정해 의료계의 반발을 불러왔다.
고시에 따르면, 제2형 당뇨병(인슐린-비의존성 당뇨병) 환자에게 투여되는 경구용 당뇨병치료제 단독요법에서 메트포민 단독투여만을 인정하는 일반원칙은 동일하다.
다만, 메트포민 단독요법 기준은 당화혈색소 6.5% 이상을 포함해 ▲공복혈당 130mg/dl 이상 ▲당뇨의 전형적인 증상과 임의혈장혈당 200mg/dl 이상▲75g 경구당부하검사 후 2시간 혈장혈당 200mg/dl 이상 등의 투여기준을 추가했다.
또한 메트포민 투여금기 환자 또는 부작용으로 메트포민을 투여할 수 없는 경우 설포닐우레아계 약제의 단독투여를 인정했다.
이 경우 기존 고시안의 의사소견서 첨부를 급여청구란에 기재하는 ‘투여소견’으로 변경했다.
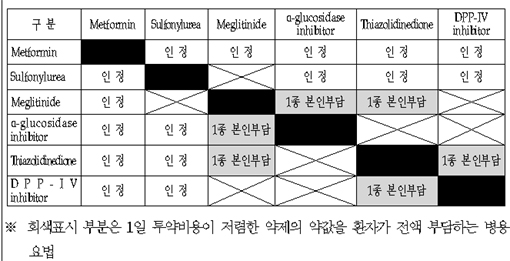
인정 가능한 당뇨병치료제 2제 요법.
병용요법도 급여기준안도 변경됐다.
기존 고시안에는 단독요법 3개월 이상 투약해도 당화혈색소가 7% 이상일 경우 의사소견서 첨부를 전제로 병용요법을 인정했다.
고시에는 단독요법 2~4개월 이상 투여으로 투여기간이 늘어났으며 병용요법 기준도 당화혈색소 7% 이상, 공복혈당 130mg/dl, 식후혈당 180mg/dl 등으로 바뀌었다.
인슐린 요법 급여기준도 확대됐다.
단독요법 중 경구용 당뇨병 치료제 병용투여에도 당화혈색소가 7% 이상인 경우 인슐린 요법을 인정하는 조항이 신설됐다.
보험약제과 관계자는 “학회와 개원의단체 등의 의견을 수렴해 소견서 첨부 등 급여청구 절차상의 문제를 완화했다”면서 “진단기준도 당뇨병학회의 가이드라인을 그대로 적용해 당화혈색소 외 혈당수치도 반영했다”고 말했다.
그는 “이번 고시는 근거중심 투여기준을 원칙으로 보장성 강화차원에서 추진된 것으로 약 90억~100억원의 재정이 추가 소요될 것”이라고 덧붙였다.

앞서 복지부는 지난 3월말 약제 고시 개정안을 통해 메트포민 단독투여를 원칙으로 당화혈색소 기준만을 적용하고 약제 변경시 의사소견서를 첨부하도록 규정해 의료계의 반발을 불러왔다.
고시에 따르면, 제2형 당뇨병(인슐린-비의존성 당뇨병) 환자에게 투여되는 경구용 당뇨병치료제 단독요법에서 메트포민 단독투여만을 인정하는 일반원칙은 동일하다.
다만, 메트포민 단독요법 기준은 당화혈색소 6.5% 이상을 포함해 ▲공복혈당 130mg/dl 이상 ▲당뇨의 전형적인 증상과 임의혈장혈당 200mg/dl 이상▲75g 경구당부하검사 후 2시간 혈장혈당 200mg/dl 이상 등의 투여기준을 추가했다.
또한 메트포민 투여금기 환자 또는 부작용으로 메트포민을 투여할 수 없는 경우 설포닐우레아계 약제의 단독투여를 인정했다.
이 경우 기존 고시안의 의사소견서 첨부를 급여청구란에 기재하는 ‘투여소견’으로 변경했다.

기존 고시안에는 단독요법 3개월 이상 투약해도 당화혈색소가 7% 이상일 경우 의사소견서 첨부를 전제로 병용요법을 인정했다.
고시에는 단독요법 2~4개월 이상 투여으로 투여기간이 늘어났으며 병용요법 기준도 당화혈색소 7% 이상, 공복혈당 130mg/dl, 식후혈당 180mg/dl 등으로 바뀌었다.
인슐린 요법 급여기준도 확대됐다.
단독요법 중 경구용 당뇨병 치료제 병용투여에도 당화혈색소가 7% 이상인 경우 인슐린 요법을 인정하는 조항이 신설됐다.
보험약제과 관계자는 “학회와 개원의단체 등의 의견을 수렴해 소견서 첨부 등 급여청구 절차상의 문제를 완화했다”면서 “진단기준도 당뇨병학회의 가이드라인을 그대로 적용해 당화혈색소 외 혈당수치도 반영했다”고 말했다.
그는 “이번 고시는 근거중심 투여기준을 원칙으로 보장성 강화차원에서 추진된 것으로 약 90억~100억원의 재정이 추가 소요될 것”이라고 덧붙였다.

관련기사
- 당뇨병약 처방 때 의사 소견서 첨부 의무화 2011-04-01 12:41:10
- 의사 소견서 갈등의 씨앗, 당뇨 급여기준 발목 2011-04-06 13:13:56
- 당뇨약 급여기준 '의사소견서→투여소견' 수정 2011-05-23 06:49:54









