- 정책
- 제도・법률
체외진단·유전자검사, 신의료기술평가 제외대상 확대
복지부, 원리와 분석대상 포괄 적용 "시장진입 5개월 단축 효과"

이창진 기자
기사입력: 2016-05-13 12:00:59
-
가
검사 분야 신의료기술평가 제외대상이 대폭 확대된다.

보건복지부(장관 정진엽)는 13일 보도참고자료를 통해 "체외진단과 유전자검사 등 검사분야 신의료기술평가 제외 대상을 확대하고, 평가기간을 기존 280일에서 140일로 대폭 단축하는 방안을 추진한다"고 밝혔다.
이번 조치는 지난해 11월 제4차 규제개혁장관회의에서 발표한 신의료기술평가 간소화 및 신속화 방안의 후속조치로 풀이된다.
신의료기술평가 대상은 기존 78%에서 29%로 축소되고, 바로 시장진입이 가능한 기존 기술은 22%에서 71%로 확대될 것으로 예상했다.
평가 제외대상 확대 기준은 검사의 핵심원리가 동일한 것은 하나의 검사 원리로 포괄해 전혀 새로운 검사법만 평가하도록 개선했다.
이를 적용하면, 기존 40개인 검사원리 분류가 16개로 줄어드는 셈이다.
또한 개별 분석물질 변경시마다 평가했으나 질환 진단을 위한 필수 물질군 변경 시에만 평가하도록 개선한다.
침과 혈액 등 검체 변경 시에도 검사 목적과 검사원리 등이 동일한 경우 평가대상에서 제외한다.
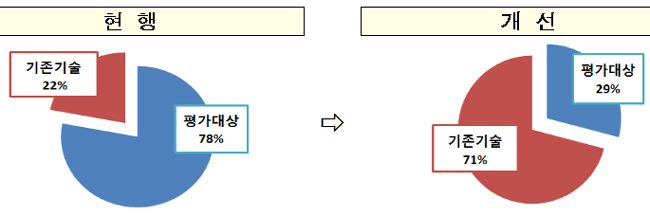
검사분야 평가 제외대상 효과.
더불어 개별 검사항목 등 미확인 물질이 포함되더라도 필수 물질군이 포함된 경우 그리고 선천성 희귀질환 판별을 위한 유전자 검사(연간 약 20건)는 남용 우려가 없는 점과 환자 접근성 등을 고려해 평가대상에서 제외한다.
복지부는 평가기간을 280일에서 140일로 감축하면, 시장진입 시기가 약 5개월 빨라질 것으로 기대했다.
의료자원정책과(과장 임을기) 관계자는 "현재 신의료기술평가 관련 규칙과 규정 개정안을 입법예고 중으로 폭넓은 의견수렴을 거쳐 개정안을 확정할 예정"이라고 말했다.

이번 조치는 지난해 11월 제4차 규제개혁장관회의에서 발표한 신의료기술평가 간소화 및 신속화 방안의 후속조치로 풀이된다.
신의료기술평가 대상은 기존 78%에서 29%로 축소되고, 바로 시장진입이 가능한 기존 기술은 22%에서 71%로 확대될 것으로 예상했다.
평가 제외대상 확대 기준은 검사의 핵심원리가 동일한 것은 하나의 검사 원리로 포괄해 전혀 새로운 검사법만 평가하도록 개선했다.
이를 적용하면, 기존 40개인 검사원리 분류가 16개로 줄어드는 셈이다.
또한 개별 분석물질 변경시마다 평가했으나 질환 진단을 위한 필수 물질군 변경 시에만 평가하도록 개선한다.
침과 혈액 등 검체 변경 시에도 검사 목적과 검사원리 등이 동일한 경우 평가대상에서 제외한다.

복지부는 평가기간을 280일에서 140일로 감축하면, 시장진입 시기가 약 5개월 빨라질 것으로 기대했다.
의료자원정책과(과장 임을기) 관계자는 "현재 신의료기술평가 관련 규칙과 규정 개정안을 입법예고 중으로 폭넓은 의견수렴을 거쳐 개정안을 확정할 예정"이라고 말했다.

관련기사
- 박 대통령 "규제개선 통해 세계적 바이오 기업 창출해야" 2016-04-21 16:21:43
- 지방흡입 시술 후 폐기된 인체지방 콜라겐 등 재활용 2016-04-27 17:24:49









