- 제약·바이오
- 국내사
식약청, DBP 부형제 단계적 퇴출
"안전성 우려 있는 성분 굳이 쓸 필요 없어"

이석준 기자
기사입력: 2009-12-28 10:06:00
-
가
앞으로 1년간 인체에서 의약품이 녹는 속도를 조절하기 위해 코팅제로 쓰이는 디부틸프탈레이트(이하 DBP) 부형제가 단계적으로 퇴출된다.
이에 따라 DBP 함유 의약품을 보유한 업체들은 약효 동등성을 유지하는 선에서 DBP를 1년 이내에 제거하거나 다른 성분으로 대체해야 한다.
식약청은 28일 이같은 내용을 뼈대로 하는 '제조(수입)품목 허가사항 변경지시'를 발표했다. 이는 DBP 관련 국외 안전성 정보에 대한 중앙약심 자문 등 종합 검토결과에 따른 것이다.
식약청 의약품관리과 김상봉 사무관은 28일 본지 통화에서 "DBP는 기계로 말하면 부품"이라며 "약효 때문에 이 성분을 써야 한다면 모르겠지만, 부형제이기 때문에 굳이 우려가 있는 성분을 쓸 이유가 없다"며 변경 사유를 답했다.
김 사무관은 "DBP 부형제를 함유한 의약품은 약효 동등성을 유지하는 선에서 1년 이내 제거하거나 다른 성분으로 대체하도록 권고한다"면서도 "단 기한은 1년을 기점으로 그 시점에서 다시 판단을 할 것이다. 1년 이내에 강제적으로 퇴출하는 것은 아니다"고 덧붙였다.
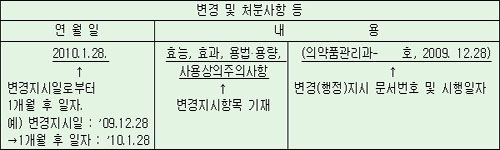
허가사항 변경지시 내용
또 식약청은 이 성분이 함유된 변비약 '둘코락스에스 장용정', 감기약 '헤브론에프 정' 등 37품목의 설명서에 DBP 생식독성 가능성을 1개월 이내에 명시토록 했다.
김 사무관은 "DBP는 덴마크 등 일부 국가에서는 이미 사용이 중단됐지만 미국, 일본 등에서는 여전히 쓰이고 있다"며 "심각한 독성은 없지만 DBP가 의약품 주성분이 아닌 부성분인 만큼, 안전성 논란이 없는 다른 부성분으로 대체키로 결정한 것"이라고 말했다.
한편, 식약청은 앞서 지난 2007년 의약품 허가심사 가이드라인을 통해 DBP 사용을 자제할 것을 권장한 바 있다.
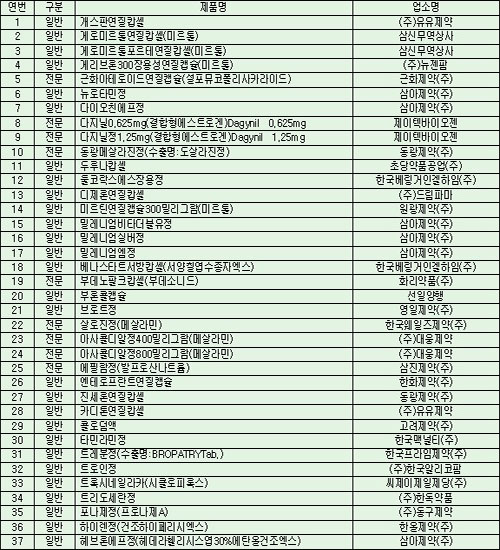
해당업소 및 품목현황
이에 따라 DBP 함유 의약품을 보유한 업체들은 약효 동등성을 유지하는 선에서 DBP를 1년 이내에 제거하거나 다른 성분으로 대체해야 한다.
식약청은 28일 이같은 내용을 뼈대로 하는 '제조(수입)품목 허가사항 변경지시'를 발표했다. 이는 DBP 관련 국외 안전성 정보에 대한 중앙약심 자문 등 종합 검토결과에 따른 것이다.
식약청 의약품관리과 김상봉 사무관은 28일 본지 통화에서 "DBP는 기계로 말하면 부품"이라며 "약효 때문에 이 성분을 써야 한다면 모르겠지만, 부형제이기 때문에 굳이 우려가 있는 성분을 쓸 이유가 없다"며 변경 사유를 답했다.
김 사무관은 "DBP 부형제를 함유한 의약품은 약효 동등성을 유지하는 선에서 1년 이내 제거하거나 다른 성분으로 대체하도록 권고한다"면서도 "단 기한은 1년을 기점으로 그 시점에서 다시 판단을 할 것이다. 1년 이내에 강제적으로 퇴출하는 것은 아니다"고 덧붙였다.

김 사무관은 "DBP는 덴마크 등 일부 국가에서는 이미 사용이 중단됐지만 미국, 일본 등에서는 여전히 쓰이고 있다"며 "심각한 독성은 없지만 DBP가 의약품 주성분이 아닌 부성분인 만큼, 안전성 논란이 없는 다른 부성분으로 대체키로 결정한 것"이라고 말했다.
한편, 식약청은 앞서 지난 2007년 의약품 허가심사 가이드라인을 통해 DBP 사용을 자제할 것을 권장한 바 있다.


제약·바이오 기사
- 제약업, 이중삼중 약가규제 속에서도 지속 성장 2009-12-28 10:00:15
- 한미약품 '아모잘탄', MR 디테일 가장 활발 2009-12-28 06:45:44
- "공정경쟁규약 개정, 리베이트 척결 계기 될 것" 2009-12-27 20:44:22
- SK케미칼, MJ사 천연팩 20종 국내 런칭 2009-12-27 20:30:52
- 종양 씨앗 세포, 제거한 자리에 종양 재발 유도해 2009-12-27 17:38:26









