오는 6월부터 단일특허제도 및 통합특허법원 시행
바이오시밀러 분야 특허 소송 등 대응변화 불가피
유럽 통합특허법원에 대한 협정(Agreement on a Unified Patent Court, UPCA) 발표 조건이 충족되면서 국내 제약바이오기업의 부담도 커질 것으로 전망된다. 유럽 진출을 위한 특허 전략의 방향성이 중요해졌다는 의미.

23일 한국바이오협회에 따르면 독일의 비준으로 유럽 통합특허법원에 대한 협정(UPCA) 발효 조건이 완료된 것으로 확인됐다.
유럽 단일특허패키지는 기존 유럽 특허 허가 시스템 강화하기 위해 유럽 전역에서의 특허보호 및 분쟁 해결에 대한 비용 투입 대비 효율성에 대한 내용이 담겨 있다.
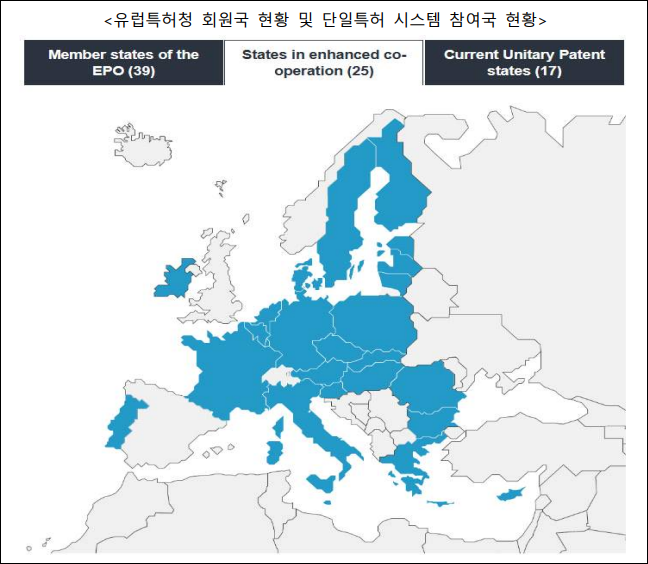
오는 6월부터 시행되는 유럽 단일특허(Unitary Patent) 신청제도는 유럽특허청(EPO)에 한 번의 요청으로 EU 25개국에서 특허 보호를 받을 수 있어 특허 신청자에게 절차적으로 간단하고 비용 효과적이라고 평가 받고 있다.
기존 유럽의 특허제도는 유럽특허청(EPO)에 특허출원을 한 자가 유럽특허청의 38개 회원국 중에서 자신이 원하는 국가를 하나 이상 선택해 개별 국가에 각각 번역문을 제출해 특허를 등록해야 했다.
다만, 이 과정을 위해서는 국가마다 다른 특허 유효화(밸리데이션) 조건과 절차를 맞춰야 한다는 점에서 직, 간접인 비용이 발생하는 어려움이 있었다.
새롭게 추가된 단일특허제도는 EU회원국 중에서 이 제도에 서명한 25개국에서 동일한 효력을 갖는 것은 물론 단일특허 출원, 심사 및 등록에 대한 수수료와 번역비 등에 있어 큰 비용 절감 효과가 기대되고 있다.
특히, 통합특허법원(Unified Patent Court)은 단일특허 및 유럽특허의 침해 및 유효성을 다루기 위해 설립된 법원으로 기존 회원국마다 병렬적으로 특허 소송하는데 드는 비용을 줄이고 법적인 명확성을 높일 수 있을 것으로 전망된다.
즉, 새로운 시스템을 통해 유럽특허청에 단일특허 신청을 하면 참여하는 모든 EU 회원국에서 특허보호가 가능하고 통합특허법원을 통해 EU 차원의 특허 소송도 가능해진다는 의미다.
이에 대해 유럽특허청장은 "유럽에서 지식재산권(IP) 보호에 대한 새로운 시대가 열렸으며, 유럽의 기업들이 낮은 비용으로 더 효율적인 특허 보호 혜택을 받을 수 있게 됐다"고 밝혔다.
하지만 유럽 시장에 진출하기 위한 바이오시밀러 분야나 새롭게 특허출원을 노리는 국내 제약바이오 기업은 향후 유럽 진출을 위한 특허 전략을 어떻게 구상할지에 대한 과제가 남아있다.
실제 의약품, 의료기기 등 바이오헬스 제품은 허가가 되면 특허에 의해 보호를 받으며 독점적으로 시장 확대가 가능하다는 점에서 특허분쟁이 많은 상황이다.
특히 바이오시밀러 분야는 가장 치열하게 특허전쟁이 벌어지는 분야로 현지 규제당국의 판매 허가를 받는 것과 별도로 오리지널의약품 개발사의 특허 공세를 무력화시켜야 하는 과정이 필요하다.
기존 유럽특허제도는 특허분쟁이 발생할 경우 각 국가마다 특허소송을 제기해야하는 번거로움과 복잡한 측면이 있었지만 동일한 특허소송에 대해 엇갈린 판결이 나오는 경우 자신에게 유리한 법리가 형성된 국가를 선택할 수 있다는 장점도 존재했다.
하지만 새로운 제도에 따라 단일특허에 대한 특허 소송이 진행될 경우 그 결과는 모든 25개 EU 참여국에 일괄 적용되게 된다.
한국바이오협회는 "유럽에서 새로운 특허제도가 추가로 시행되는 만큼 특허를 등록할 기업들은 현재와 미래를 보고 전략적으로 어떤 특허제도를 선택할지 고민해야 한다"며 "이들 기업들과 특허 소송을 해야 하는 기업들은 어떻게 대응할지 고민해야 하는 복잡한 상황이 전개될 것으로 보인다"고 덧붙였다.








