- 제약·바이오
- 국내사
"1400억 타깃" 비리어드 염변경 제네릭 대거 허가
발행날짜: 2017-08-14 04:54:11
-
가
-
식약처, 19개 품목 허가…보험등재 기간, 조기 출시 변수
국산 제네릭이 식품의약품안전처의 품목 허가를 받고 1400억원에 달하는 B형간염 치료제 비리어드의 시장을 뺏기위한 출격 대기에 들어갔다.
특히 이번 품목 허가에서 오리지널의 성분인 테노포비르디소프록실푸마르산염에서 염을 변경한 제네릭이어서 특허 만료일인 11월 이전 출시 가능성도 높아지고 있다.
식품의약품안전처에 따르면 11일 하루에만 국내 제약사 19곳이 비리어드 제네릭의 품목 승인을 얻은 것으로 나타났다.
길리어드의 B형간염 치료제 '비리어드'는 한해 1400억원의 매출을 올린 대형 블록버스터 약물.
B형간염 치료제 시장 점유율 절반 이상을 차지하면서 국내 제약사의 복제약 타깃이 됐다.
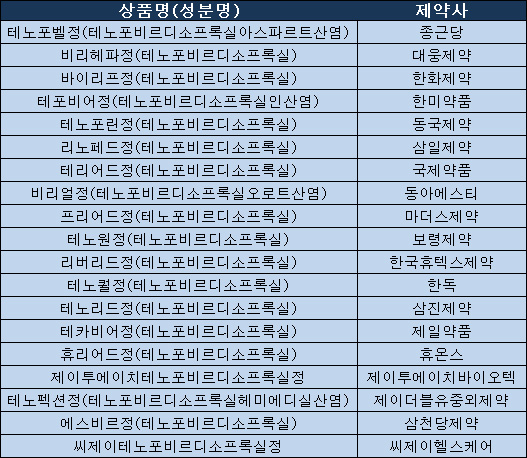
비리어드 제네릭을 승인받은 제약사는 종근당 테노포벨정, 대웅제약 비리헤파정, 한화제약 바이리프정, 한미약품 테포비어정, 동국제약 테노포린정, 동아에스티 비리얼정, 보령제약 테노원정, 한독 테노퀄정, 삼진제약 테노리드정, 제일약품 테카비어정, JW중외제약 테노펙션정, CJ헬스케어 CJ테노포비르디소프록실정 등 19개 품목이다.
오리지널 비리어드의 성분은 테노포비르디소프록실푸마르산염.
반면 이번에 13개 제약사는 테노포비르디소프록실 성분으로 허가를 얻었고, 나머지 종근당이 아스파르트산염으로, 한미약품이 인산염으로, 동아에스티가 오로트산염, JW중외제약이 헤미에디실산염으로 각각 허가를 얻었다.
염 변경 제네릭이 대거 출현한 것은 특허 회피와 관련이 있다.
비리어드의 물질특허는 오는 11월까지 유지되지만, 염 변경된 품목이 연장된 물질특허에 영향을 받지 않는다는 판결이 최근 나오면서 국내 제약사들이 염 변경을 통한 제네릭 조기 출시 가능성이 높아졌다.
실제로 지난 특허심판원은 한미약품, 삼진제약, 보령제약, 삼일제약 등 8개 제약사가 제기한 비리어드의 뉴클레오타이드 동족체 관련 소극적 권리범위 확인 청구에서 국내 제약사의 손을 들어준 바 있다.
제네릭 조기 출시에 장애물은 사라진 셈이지만 문제는 품목 허가 이후 보험급여 등재까지의 기간이다.
통상 보험급여 등재까지 2~3개월 걸리는 점을 감안하면 11월 특허 만료 전 제네릭의 조기 출시 기간이 불과 한 달 남짓에 불과해 실익이 없을 수 있다는 전망도 나온다.
특히 이번 품목 허가에서 오리지널의 성분인 테노포비르디소프록실푸마르산염에서 염을 변경한 제네릭이어서 특허 만료일인 11월 이전 출시 가능성도 높아지고 있다.
식품의약품안전처에 따르면 11일 하루에만 국내 제약사 19곳이 비리어드 제네릭의 품목 승인을 얻은 것으로 나타났다.
길리어드의 B형간염 치료제 '비리어드'는 한해 1400억원의 매출을 올린 대형 블록버스터 약물.
B형간염 치료제 시장 점유율 절반 이상을 차지하면서 국내 제약사의 복제약 타깃이 됐다.

오리지널 비리어드의 성분은 테노포비르디소프록실푸마르산염.
반면 이번에 13개 제약사는 테노포비르디소프록실 성분으로 허가를 얻었고, 나머지 종근당이 아스파르트산염으로, 한미약품이 인산염으로, 동아에스티가 오로트산염, JW중외제약이 헤미에디실산염으로 각각 허가를 얻었다.
염 변경 제네릭이 대거 출현한 것은 특허 회피와 관련이 있다.
비리어드의 물질특허는 오는 11월까지 유지되지만, 염 변경된 품목이 연장된 물질특허에 영향을 받지 않는다는 판결이 최근 나오면서 국내 제약사들이 염 변경을 통한 제네릭 조기 출시 가능성이 높아졌다.
실제로 지난 특허심판원은 한미약품, 삼진제약, 보령제약, 삼일제약 등 8개 제약사가 제기한 비리어드의 뉴클레오타이드 동족체 관련 소극적 권리범위 확인 청구에서 국내 제약사의 손을 들어준 바 있다.
제네릭 조기 출시에 장애물은 사라진 셈이지만 문제는 품목 허가 이후 보험급여 등재까지의 기간이다.
통상 보험급여 등재까지 2~3개월 걸리는 점을 감안하면 11월 특허 만료 전 제네릭의 조기 출시 기간이 불과 한 달 남짓에 불과해 실익이 없을 수 있다는 전망도 나온다.
관련기사
- 비리어드 특허 구멍…제네릭 조기 출시 가능성↑ 2017-07-20 11:43:31
- 비리어드 떼어내기…베믈리디VS베시보 신약 경쟁 2017-06-26 05:00:53
- '비리어드'도 못 비켜간 내성 발현…국내 2명 확증 2017-06-24 12:00:00
- 베시보 야심찬 출사표? 복약순응도·베믈리디 복병 2017-05-23 05:00:10






