- 정책
- 제도・법률
뇌경막 이식환자 CJD 감염 "인간광우병 아니다"
질병관리본부, 추적조사…식약청 "라이오듀라 수입 전무"

이창진 기자
기사입력: 2011-11-29 11:34:52
-
가
뇌경막 이식 후 사망 환자에서 CJD(크로이츠펠트-야콥병) 감염 사례가 처음으로 발견됐다.

질병관리본부(본부장 전병율)는 29일 "뇌경막을 이식받은 병력이 있는 환자의 조직검사 및 동물실험 결과, 치료과정에서 발생한 의인성 CJD 사례를 확인했다"고 밝혔다.
이번 사례는 54세 여성으로 1987년 뇌수막종 치료 중 독일제 수입 뇌경막(Lyodura, 라이요두라)을 이식받았으며, 수술 후 2010년 6월 발병해 산발성 CJD 의심환자로 신고돼 조사가 진행 중이던 같은 해 11월 사망했다.
이같은 결과는 한림의대 김윤중 교수팀이 대한의학회지 11월호에 발표해 알려졌다.
질병관리본부는 의인성 CJD는 감염된 조직 이식 등 의학적 치료과정에서 발생할 수 있는 CJD로 인간광우병으로 알려진 변종 CJD와는 무관하다고 강조했다.
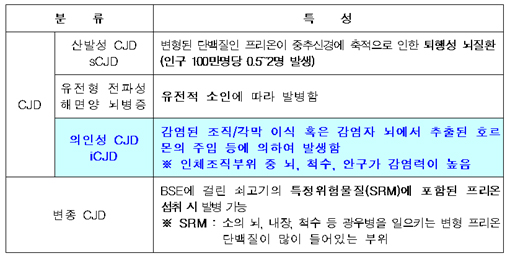
크로이츠펠트-야콥병 분류.
본부측은 환자에게 이식된 독일제 수입 뇌경막은 산발성 CJD에 감염된 환자 사체에서 적출된 뇌경막을 사용한 것으로 추정된다고 설명했다.
문제가 된 독일제 뇌경막은 1987년 이후 프리온(단백질 한 종류) 감염력을 제거하기 위한 불활성화 처리해 사용하고 있는 상태이다.
현재 경막대용제로 수술시 사용되는 수입 제품은 5개 제품(4개 회사)으로 국내외 사례 및 생산공정 등을 감안할 때 CJD 유발 가능성이 없다는 입장이다.
다만, 라이오두라를 이식받은 환자의 규모는 정확히 알 수 없으나 이번 사례 외에도 이식 사례가 있을 가능성이 있어 CJD 발생 가능성에 대한 추가 조사가 필요하다고 덧붙였다.
감염병관리과는 "첫 의인성 CJD 사례가 발견됨에 따라 신경과 및 신경외과 학회 등과 협조체계를 구축했다"면서 "80년대 뇌경막 이식 환자의 동의를 전제로 의무기록 확인 및 신경학적 검사 등 추적조사를 추진하고 있다"고 말했다.
한편 식약청은 "라이오듀라 제품은 소의 뇌조직이 아닌 인체의 경막을 원료로 제조한 제품으로, 1987년 이후 제조 판매가 중단된 상태"라면서 "국내에는 허가된 바 없다"고 밝혔다.
또 식약청은 "1998년부터 동물 유래조직 또는 합성고분자 물질을 이용해 제조한 제품을 안전성 유효성 검사를 거쳐 안전성이 확인된 경우 경막대용재로 허가하고 있다"고 환기시켰다.
이어 식약청은 "이 경막대용재는 수입 통관할 때 전염성해면상뇌증(TSE) 미감염증명서 제출을 의무화하고 있다. 현재 의료기관에서 사용중인 제품은 라이오듀라가 아닌 동일 제조원의 '라이오플란드'로서 식약청이 안전성을 확인한 제품"이라고 확인했다.

이번 사례는 54세 여성으로 1987년 뇌수막종 치료 중 독일제 수입 뇌경막(Lyodura, 라이요두라)을 이식받았으며, 수술 후 2010년 6월 발병해 산발성 CJD 의심환자로 신고돼 조사가 진행 중이던 같은 해 11월 사망했다.
이같은 결과는 한림의대 김윤중 교수팀이 대한의학회지 11월호에 발표해 알려졌다.
질병관리본부는 의인성 CJD는 감염된 조직 이식 등 의학적 치료과정에서 발생할 수 있는 CJD로 인간광우병으로 알려진 변종 CJD와는 무관하다고 강조했다.

문제가 된 독일제 뇌경막은 1987년 이후 프리온(단백질 한 종류) 감염력을 제거하기 위한 불활성화 처리해 사용하고 있는 상태이다.
현재 경막대용제로 수술시 사용되는 수입 제품은 5개 제품(4개 회사)으로 국내외 사례 및 생산공정 등을 감안할 때 CJD 유발 가능성이 없다는 입장이다.
다만, 라이오두라를 이식받은 환자의 규모는 정확히 알 수 없으나 이번 사례 외에도 이식 사례가 있을 가능성이 있어 CJD 발생 가능성에 대한 추가 조사가 필요하다고 덧붙였다.
감염병관리과는 "첫 의인성 CJD 사례가 발견됨에 따라 신경과 및 신경외과 학회 등과 협조체계를 구축했다"면서 "80년대 뇌경막 이식 환자의 동의를 전제로 의무기록 확인 및 신경학적 검사 등 추적조사를 추진하고 있다"고 말했다.
한편 식약청은 "라이오듀라 제품은 소의 뇌조직이 아닌 인체의 경막을 원료로 제조한 제품으로, 1987년 이후 제조 판매가 중단된 상태"라면서 "국내에는 허가된 바 없다"고 밝혔다.
또 식약청은 "1998년부터 동물 유래조직 또는 합성고분자 물질을 이용해 제조한 제품을 안전성 유효성 검사를 거쳐 안전성이 확인된 경우 경막대용재로 허가하고 있다"고 환기시켰다.
이어 식약청은 "이 경막대용재는 수입 통관할 때 전염성해면상뇌증(TSE) 미감염증명서 제출을 의무화하고 있다. 현재 의료기관에서 사용중인 제품은 라이오듀라가 아닌 동일 제조원의 '라이오플란드'로서 식약청이 안전성을 확인한 제품"이라고 확인했다.

정책 기사
- "공보의 수급 오락가락, 지침 안고치고 땜질만" 2011-11-29 06:40:34
- 복지부 "저질 요양병원 퇴출…옥석 가리겠다" 2011-11-28 12:40:18
- 한국간호평가원, 2012년부터 간호대학 인증평가 2011-11-28 11:53:57
- 국회 먹통 장기화 조짐…의료계 주요법안 낮잠 2011-11-28 11:45:34
- 멱살잡이에 욕설까지…'사각지대' 놓인 공보의들 2011-11-28 06:40:56









