- 정책
- 제도・법률
"위해성 높은 3ㆍ4등급 의료기기 부실심사"
김정록 의원 "서류심사로 대체 2년간 172건" 지적

정희석 기자
기사입력: 2013-10-21 12:17:34
-
가
의료기기 제조 및 품질관리(GMP) 부실심사가 도마위에 올랐다.

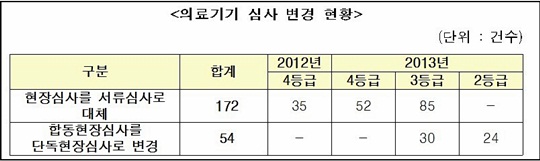
새누리당 김정록 의원(보건복지위)은 최근 2년간 의료기기 심사 신청 건수 중 현장심사 대상이지만 서류심사로 대체된 것이 2012년 35건에 이어 올해 137건에 달한다고 지적했다.
김 의원에 따르면, 서류심사로 대체된 의료기기를 등급별로 구분하면 잠재적 위해성이 높은 3등급ㆍ4등급이 각각 85건과 87건으로 집계됐다.
철저한 관리가 필요한 3ㆍ4등급 의료기기를 아무런 현장심사 없이 서류심사만으로 관리하는 건 심각한 문제라는 지적이다.
현행 '의료기기 제조 및 품질관리기준' 제8조 3항에 의해 의료기기 정기갱신 심사는 서류검토 및 현장심사를 실시토록 돼 있다.
또 'GMP 심사 세부운영 가이드라인'에는 정기갱신검사 또는 변경심사의 경우 제조소별로 심사를 하도록 규정돼있다.
문제는 GMP 심사 세부운영 가이드라인조차 서로 상반된 심사기준을 적용하고 있는 것.
그는 "가이드라인에는 정기갱신검사에서 2개 이상 제조소에서 제조된 의료기기를 수입하는 수입자의 경우 경비ㆍ인력을 고려해 1개 제조소에 대해서만 현장심사를 실시하고 나머지는 서류심사로 대체한다고 돼 있다"고 지적했다.
김정록 의원은 "현재 GMP 심사 세부운영 가이드라인이 서로 상반된 기준을 적용하고 있어 적절한 심사가 이뤄지지 않고 있다"며 "가이드라인에 맞도록 고시를 개정하거나 가이드라인 자체를 손질할 필요성이 있다"고 식약처에 주문했다.

김 의원에 따르면, 서류심사로 대체된 의료기기를 등급별로 구분하면 잠재적 위해성이 높은 3등급ㆍ4등급이 각각 85건과 87건으로 집계됐다.
철저한 관리가 필요한 3ㆍ4등급 의료기기를 아무런 현장심사 없이 서류심사만으로 관리하는 건 심각한 문제라는 지적이다.
현행 '의료기기 제조 및 품질관리기준' 제8조 3항에 의해 의료기기 정기갱신 심사는 서류검토 및 현장심사를 실시토록 돼 있다.
또 'GMP 심사 세부운영 가이드라인'에는 정기갱신검사 또는 변경심사의 경우 제조소별로 심사를 하도록 규정돼있다.
그는 "가이드라인에는 정기갱신검사에서 2개 이상 제조소에서 제조된 의료기기를 수입하는 수입자의 경우 경비ㆍ인력을 고려해 1개 제조소에 대해서만 현장심사를 실시하고 나머지는 서류심사로 대체한다고 돼 있다"고 지적했다.
김정록 의원은 "현재 GMP 심사 세부운영 가이드라인이 서로 상반된 기준을 적용하고 있어 적절한 심사가 이뤄지지 않고 있다"며 "가이드라인에 맞도록 고시를 개정하거나 가이드라인 자체를 손질할 필요성이 있다"고 식약처에 주문했다.

정책 기사
- 대형병원 수입 '널뛰기'…8월 진료비 31% 수직하락 2013-10-21 11:59:45
- "치매병력 인체조직 '묻지마' 환자 이식" 2013-10-21 11:20:55
- 심평원, 보건복지가족 한마음 야구대회 개최 2013-10-20 21:37:18
- 20대 여성 치질 환자, 남성보다 17% 더 많다 2013-10-20 21:30:41
- "식약처 정보비공개 비율 91%, 국민 알권리 침해" 2013-10-20 15:24:15









