- 제약·바이오
- 국내사
올 상반기 13개 제품 신약 허가…국내사 '0'
식약청 의약품 허가 현황 발표, 원료의약품 중국산 많아

박진규 기자
기사입력: 2009-07-24 10:39:50
-
가
식품의약품안전청은 올해 상반기(1~6월) 동안 허가된 의약품의 현황을 분석한 결과 총 2612품목으로 작년 상반기 3464품목에 비해 24.6% 감소한 것으로 나타났다고 14일 밝혔다.
특히 전문의약품의 허가 감소(2008년 대비 994품목) 경향이 두드러졌는데, 작년 7월1일부터 전문의약품에 대해 품목별 사전 GMP 평가가 의무화된데 따른 것으로 분석됐다.
또 상반기 동안 희귀의약품 3건, 생물학적 제제 1건 등 총 13개 제품이 신약으로 허가됐는데 국내사는 1건도 없어 국내 제약사의 신약 개발을 위한 노력이 요구됐다.
개량신약으로 허가받은 품목은 한미약품의 아모잘탄정5/100mg 등 4품목으로 나타났다.
약효군별로 보면 질환의 치료에 사용되는 의약품보다 혼합비타민제 단백아미노산제 칼슘제 등 자양강장 관련 제품 허가가 272품목으로 전체 허가 건수의 22%를 차지했다. 이는 '해피드럭'에 다한 소비자들의 수요 증가에 따른 것으로 보인다.
항생제의 경우 52개 품목이 허가됐는데 46(88%)개는 수출용이었다. 반면 항암제는 7품목 중 5품목이 수입품목으로 대비를 이뤘다.
또 이 기간 중 273개 품목이 생동성입증 품목으로 허가 받아 생동성입증 품목은 총 6821개로 늘어났다
이와 함께 올 상반기 허가된 원료의약품의 주 수입국은 중국으로, 향후 중국 의약품 제조 및 품질관리 정책에 대한 철저한 모니터링이 요구됐다. 208품목 가운데 43%는 국내에서 제조하고 57%는 중국에서 생산된 의약품을 수입해 국내에서 포장하는 소분 제조 품목이었다.
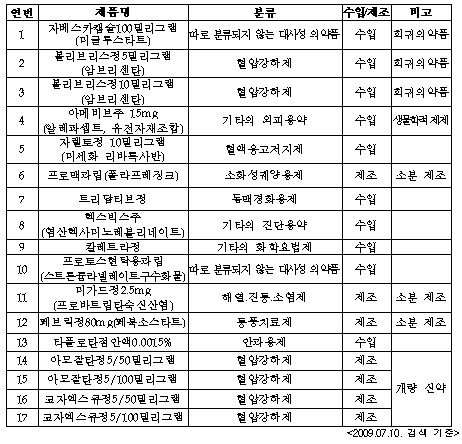
2009년 상반기 신약 및 개량신약 허가 현황
특히 전문의약품의 허가 감소(2008년 대비 994품목) 경향이 두드러졌는데, 작년 7월1일부터 전문의약품에 대해 품목별 사전 GMP 평가가 의무화된데 따른 것으로 분석됐다.
또 상반기 동안 희귀의약품 3건, 생물학적 제제 1건 등 총 13개 제품이 신약으로 허가됐는데 국내사는 1건도 없어 국내 제약사의 신약 개발을 위한 노력이 요구됐다.
개량신약으로 허가받은 품목은 한미약품의 아모잘탄정5/100mg 등 4품목으로 나타났다.
약효군별로 보면 질환의 치료에 사용되는 의약품보다 혼합비타민제 단백아미노산제 칼슘제 등 자양강장 관련 제품 허가가 272품목으로 전체 허가 건수의 22%를 차지했다. 이는 '해피드럭'에 다한 소비자들의 수요 증가에 따른 것으로 보인다.
항생제의 경우 52개 품목이 허가됐는데 46(88%)개는 수출용이었다. 반면 항암제는 7품목 중 5품목이 수입품목으로 대비를 이뤘다.
또 이 기간 중 273개 품목이 생동성입증 품목으로 허가 받아 생동성입증 품목은 총 6821개로 늘어났다
이와 함께 올 상반기 허가된 원료의약품의 주 수입국은 중국으로, 향후 중국 의약품 제조 및 품질관리 정책에 대한 철저한 모니터링이 요구됐다. 208품목 가운데 43%는 국내에서 제조하고 57%는 중국에서 생산된 의약품을 수입해 국내에서 포장하는 소분 제조 품목이었다.


제약·바이오 기사
- FDA 자문위원, 신속한 신종플루 백신 승인 원해 2009-07-24 09:58:13
- 고혈압약 베타 차단제, 백내장 위험성 높여 2009-07-24 09:39:49
- 성장인자 주사, 손상된 심장조직 재생 유도해 2009-07-24 09:37:26
- "가장 광범위한 슈퍼항생제 떴다" 2009-07-24 06:45:08
- 코자-암로디핀 장점만 한알에…'코자XQ' 출시 2009-07-23 11:11:34









