- 제약·바이오
- 국내사
다국적제약은 '항암'…국내사는 개량신약 집중
식약청 임상시험 승인 현황 분석 결과 고부가 가치-안정성 대비

정희석 기자
기사입력: 2014-02-12 06:04:10
-
가
다국적 제약사가 항암제 신약 개발에 주력하는 반면 국내사는 심혈관ㆍ내분비계 개량신약에 집중하고 있는 것으로 나타났다.
식약처가 최근 발표한 2013년도 임상시험 승인 현황을 분석한 결과다.
임상시험 승인 의약품을 효능군으로 살펴보면 ▲종양(157건) ▲심혈관계(80건) ▲내분비계(51건) ▲중추신경계(46건) 순으로 많았다.
특히 다국적 제약사와 국내사 간 집중하는 효능군별 임상 분야는 상이한 차이를 보였다.
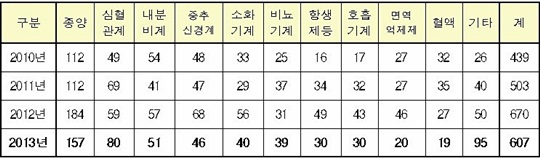
2013년 신규 승인 임상시험 효능군 현황
다국적 제약사는 항암제 개발을 위한 종양(101건) 관련 임상시험이 월등히 많았고, 심혈관계(20건)ㆍ내분비계(19건)ㆍ중추신경계(19건)ㆍ항생제(18건)가 뒤를 이었다.
반면 국내사는 심혈관계(56건)ㆍ내분비계(30건) 임상시험이 주를 이뤘다.
다국적 제약사가 고부가가치 항암제 신약 개발에 집중하는 것과 달리 비용과 시간 모두 여력이 부족한 국내사는 비용 대비 성공률이 높은 개량신약 개발에 주력하고 있는 모양새다.
지난해 임상시험 승인은 다국적 제약사 한국노바티스가 28건으로 가장 많았다.
이어 다국적 CRO 퀸타일즈 트랜스내셔널코리아와 서울대병원이 각각 25건ㆍ24건으로 2~3위를 차지했다.
국내사 중에서는 일동제약이 15건으로 9위에 이름을 올렸고, 뒤이어 종근당(14건)ㆍ한미약품(12건)이 각각 12위와 14위를 기록했다.
한편 지난해 전체 임상시험 승인건수는 총 607건으로 2012년 670건과 비교해 약 9.4%(63건) 감소한 것으로 조사됐다.
하지만 국내 제약사 임상시험 승인은 2012년 208건에서 지난해 227건으로 오히려 9.1% 증가한 것으로 나타났다.
식약처가 최근 발표한 2013년도 임상시험 승인 현황을 분석한 결과다.
임상시험 승인 의약품을 효능군으로 살펴보면 ▲종양(157건) ▲심혈관계(80건) ▲내분비계(51건) ▲중추신경계(46건) 순으로 많았다.
특히 다국적 제약사와 국내사 간 집중하는 효능군별 임상 분야는 상이한 차이를 보였다.
반면 국내사는 심혈관계(56건)ㆍ내분비계(30건) 임상시험이 주를 이뤘다.
다국적 제약사가 고부가가치 항암제 신약 개발에 집중하는 것과 달리 비용과 시간 모두 여력이 부족한 국내사는 비용 대비 성공률이 높은 개량신약 개발에 주력하고 있는 모양새다.
지난해 임상시험 승인은 다국적 제약사 한국노바티스가 28건으로 가장 많았다.
이어 다국적 CRO 퀸타일즈 트랜스내셔널코리아와 서울대병원이 각각 25건ㆍ24건으로 2~3위를 차지했다.
국내사 중에서는 일동제약이 15건으로 9위에 이름을 올렸고, 뒤이어 종근당(14건)ㆍ한미약품(12건)이 각각 12위와 14위를 기록했다.
한편 지난해 전체 임상시험 승인건수는 총 607건으로 2012년 670건과 비교해 약 9.4%(63건) 감소한 것으로 조사됐다.
하지만 국내 제약사 임상시험 승인은 2012년 208건에서 지난해 227건으로 오히려 9.1% 증가한 것으로 나타났다.

제약·바이오 기사
- 제약계, 전문약 매출 고전…분유 팔아 손실 막았다 2014-02-11 06:17:26
- 검찰, 모제약 리베이트 연루 의사 12명 불구속 기소 2014-02-10 12:14:10
- 이센트레스, HIV/AIDS 치료 1차약 권고 2014-02-10 12:04:05
- 한미약품, 12시간 지속 알레르기비염약 출시 2014-02-10 11:39:48
- 법원 "리리카 제네릭 통증 치료에 처방 못한다" 2014-02-10 11:27:22









