식약처, 11월까지 67회 실시…현장실습 중심 커리큘럼 구성
임상시험부터 국내외 규제, 최신 국제규격까지 의료기기 인허가에 필요한 전문인력 양성교육이 본격 실시된다.
식약처는 의료기기 전문인력 육성을 위해 의료기기 연구‧개발자, 인허가 업무 담당자 1000여명을 대상으로 오는 21일 의료기기정보기술지원센터에서 1차 교육을 시작으로 11월까지 전국 주요도시에서 67회에 걸친 종합교육을 진행한다.
이번 교육은 미래창조과학부·산업통상자원부 등 정부 각 부처가 지원하는 의료기기 연구개발(R&D)사업으로 개발되는 의료기기 제품화 비율을 높이고, 신속한 허가가 이뤄지도록 지원하기 위해 마련했다.
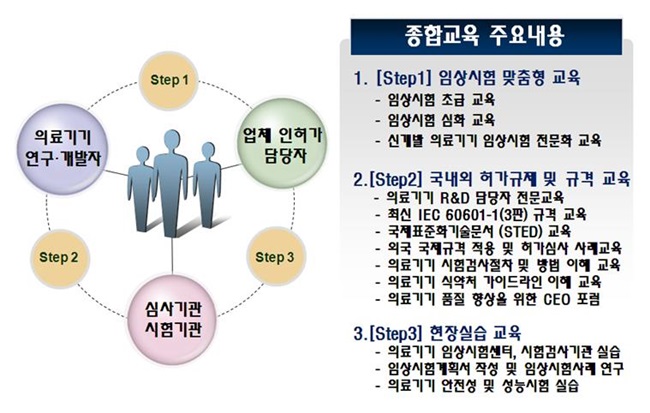
주요 교육내용은 ▲임상시험 계획서 작성법 ▲임상시험 실시·모니터링 방법 ▲안전성·성능 검증을 위한 국내외 규격과 인허가 제도 ▲의료기기 국제표준화기술문서(STED) 작성법 등이다.
특히 임상시험센터·시험검사기관 등 현장실습 중심으로 교육을 구성해 제품개발 및 인허가 시 바로 적용하고 활용할 수 있도록 했다.
식약처는 "이번 종합교육이 허가 신청용 기술문서 작성부터 국내외 규격 적용까지 인허가 전반에 대한 전문인력 인프라 확대에 기여 할 것"이라며 "앞으로도 국제적인 경쟁력을 갖춘 신개발 의료기기 제품화 실현과 신속한 시장진출을 위해 관련 교육에 앞장서겠다"고 밝혔다.
교육내용이나 일정, 참가 신청 등에 대한 자세한 사항은 의료기기정보기술지원센터 홈페이지(www.mdtac.or.kr)에서 확인할 수 있다.
식약처는 의료기기 전문인력 육성을 위해 의료기기 연구‧개발자, 인허가 업무 담당자 1000여명을 대상으로 오는 21일 의료기기정보기술지원센터에서 1차 교육을 시작으로 11월까지 전국 주요도시에서 67회에 걸친 종합교육을 진행한다.
이번 교육은 미래창조과학부·산업통상자원부 등 정부 각 부처가 지원하는 의료기기 연구개발(R&D)사업으로 개발되는 의료기기 제품화 비율을 높이고, 신속한 허가가 이뤄지도록 지원하기 위해 마련했다.
특히 임상시험센터·시험검사기관 등 현장실습 중심으로 교육을 구성해 제품개발 및 인허가 시 바로 적용하고 활용할 수 있도록 했다.
식약처는 "이번 종합교육이 허가 신청용 기술문서 작성부터 국내외 규격 적용까지 인허가 전반에 대한 전문인력 인프라 확대에 기여 할 것"이라며 "앞으로도 국제적인 경쟁력을 갖춘 신개발 의료기기 제품화 실현과 신속한 시장진출을 위해 관련 교육에 앞장서겠다"고 밝혔다.
교육내용이나 일정, 참가 신청 등에 대한 자세한 사항은 의료기기정보기술지원센터 홈페이지(www.mdtac.or.kr)에서 확인할 수 있다.







