식약처, 유럽의약품청 등 안전성 정보 반영
스타틴과 병용시 혈중 농도 증가시킬 수 있어
리피토정 등 아토르바스타틴 제제와 글레카프레비르 및 피브렌타스비르 성분 C형 감염 치료제와의 병용이 금지된다.
식품의약품안전처는 이같은 내용의 의약품 품목허가사항 변경 지시를 지난 9일 내리고 의견 제출을 요청했다.
식약처는 유럽 의약품청 및 유럽 의약품안전관리기구의 아토르바스타틴 함유제제 관련 안전성 정보에 대한 검토 결과 허가 변경을 결정했다.
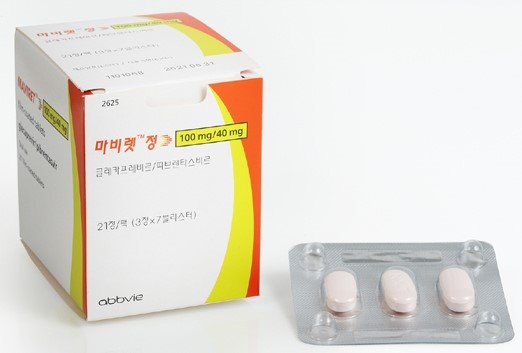
글레카프레비르 및 피브렌타스비르 성분 C형 간염 치료제는 한국애비브의 마비렛 정이 유일하다.
마비렛 정은 스타틴 계열의 로수바스타틴이나 프라바스타틴과의 병용투여시 스타틴 성분의 혈중 농도 증가로 인한 횡문근 융해증을 포함한 근육병증 위험이 높아질 수 있어 주의가 필요했다. 여기에 이상지질혈증 치료제 아토르바스타틴이 추가된 것. 대상 품목은 375개다.
식약처는 허가사항 변경지시안을 통해 아토르바스타틴 투여 금지 대상에 글레카프레비르 및 피브렌타스비르를 투여중인 환자를 추가했다. 또 이상반응에는 근육파열, 매우 드물게 루푸스양 증후군을 추가했다.
실제로 아토르바스타틴 10mg과 마비렛정(400/120mg) 1일 1회 복용시 약동학 변수는 최대혈중농도(Cmax) 값이 22, 혈중농도 곡선하면적(AUC) 값이 8.28로 약물상호작용 가능성이 높았다.
약물상호작용 가능성이 적은 경우 Cmax와 AUC는 1에 근접한다.
식약처는 24일까지 의견을 접수해 최종 허가사항을 변경한다는 방침이다.
식품의약품안전처는 이같은 내용의 의약품 품목허가사항 변경 지시를 지난 9일 내리고 의견 제출을 요청했다.
식약처는 유럽 의약품청 및 유럽 의약품안전관리기구의 아토르바스타틴 함유제제 관련 안전성 정보에 대한 검토 결과 허가 변경을 결정했다.

마비렛 정은 스타틴 계열의 로수바스타틴이나 프라바스타틴과의 병용투여시 스타틴 성분의 혈중 농도 증가로 인한 횡문근 융해증을 포함한 근육병증 위험이 높아질 수 있어 주의가 필요했다. 여기에 이상지질혈증 치료제 아토르바스타틴이 추가된 것. 대상 품목은 375개다.
식약처는 허가사항 변경지시안을 통해 아토르바스타틴 투여 금지 대상에 글레카프레비르 및 피브렌타스비르를 투여중인 환자를 추가했다. 또 이상반응에는 근육파열, 매우 드물게 루푸스양 증후군을 추가했다.
실제로 아토르바스타틴 10mg과 마비렛정(400/120mg) 1일 1회 복용시 약동학 변수는 최대혈중농도(Cmax) 값이 22, 혈중농도 곡선하면적(AUC) 값이 8.28로 약물상호작용 가능성이 높았다.
약물상호작용 가능성이 적은 경우 Cmax와 AUC는 1에 근접한다.
식약처는 24일까지 의견을 접수해 최종 허가사항을 변경한다는 방침이다.








