화이자 코미나티주 0.1mg 승인…예방효과 91%
"미국, 유럽연합, 영국 등 62개국에서 사용 중"
5~11세에 접종 가능한 코로나19 백신 옵션이 등장했다. 2회 접종으로 약 91%의 예방효과를 나타냈다.
23일 식품의약품안전처는 화이자제약이 허가 신청한 5~11세용 코로나19 백신 '코미나티주0.1mg/mL(5-11세용)'를 허가했다.
이번에 허가한 '코미나티주0.1mg/mL(5-11세용)'는 미국 화이자사와 독일 바이오엔텍사가 공동 개발하고 한국화이자제약이 수입하는 mRNA 백신이다.
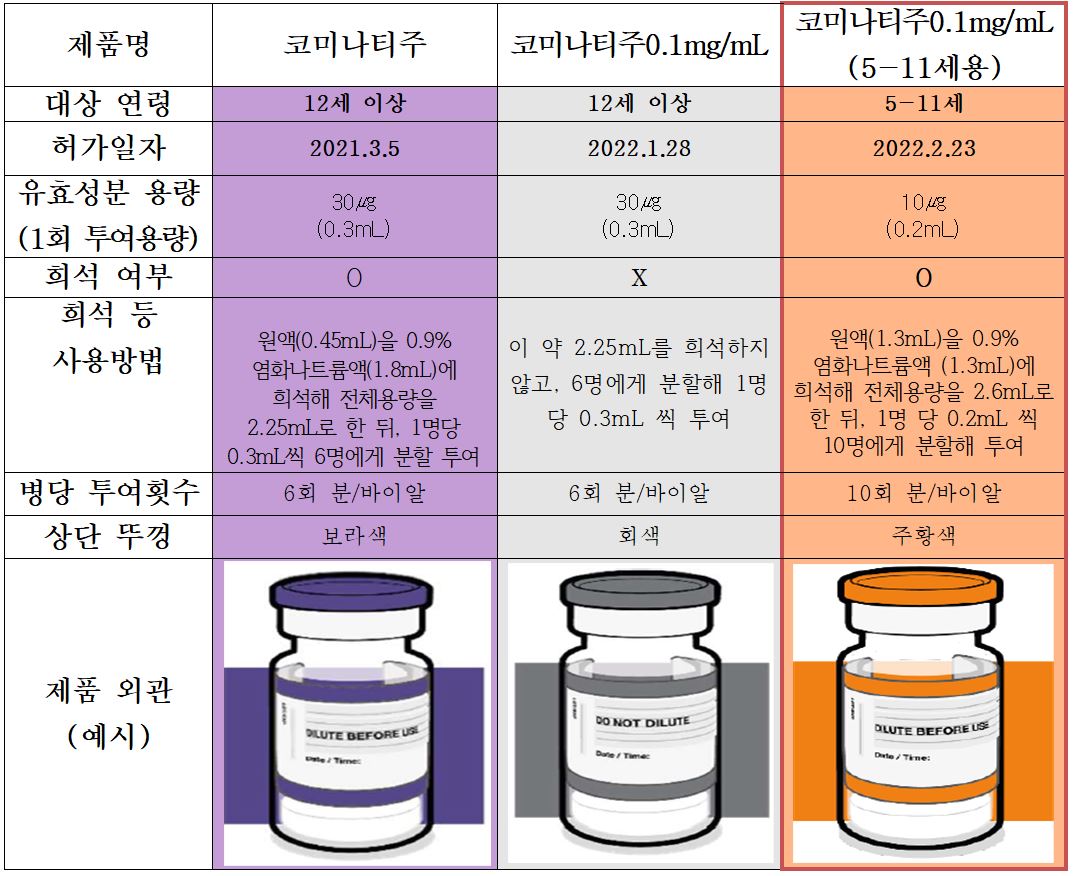
'코미나티주0.1mg/mL(5-11세용)'는 5~11세의 코로나19 예방 목적으로 미국 화이자사가 별도 개발·생산하는 백신으로, 앞서 식약처가 허가한 '코미나티주', '코미나티주0.1mg/mL'와 유효성분(토지나메란)은 같으나 용법·용량에는 차이가 있다.
이번에 허가된 백신은 최근 오미크론 변이 확산으로 코로나19 확진자가 증가하는 상황에서 어린이의 코로나19 예방 및 중증으로 악화를 방지할 수 있는 첫 백신이라는 점에서 의의가 있다.
식약처는 '코미나티주0.1mg/mL(5-11세용)'에 대한 심사 결과와 중앙약사심의위원회의 자문 등을 종합적으로 검토해, 해당 품목의 효과성과 안전성을 확인했다.
5∼11세 3109명을 대상으로 안전성을 비교해 평가했을 때, 전반적인 안전성 정보는 16∼25세(1064명)와 유사했다.
백신 접종 후 가장 빈번하게 나타나는 이상사례는 주사부위 통증, 피로, 두통, 주사부위 발적·종창, 근육통, 오한 등이었고, 증상은 대부분 경증에서 중간 정도 수준이었다.
5∼11세(264명)와 16∼25세(253명)에서 코로나19 면역반응을 비교해 평가했으며, 5∼11세에서 백신(1305명)과 대조약물(663명)을 투여한 후 코로나19 감염 환자의 비율로 예방효과를 평가했다.
2차 접종 완료 후 1개월 시점에서 5∼11세와 16∼25세의 면역반응을 비교한 결과, 중화항체가 비율과 혈청반응률 모두 효과가 입증된 것으로 나타났다.
코로나19에 감염되지 않은 1968명(시험군 1305명, 대조군 663명)을 대상으로 2차 접종 완료 7일 후 예방효과를 분석한 결과, 백신 접종에 따른 예방효과는 90.7%이었다.
식약처는 심사 결과와 중앙약사심의위원회 자문 내용을 종합적으로 검토한 결과, 임상시험 최종결과보고서 등을 허가 후 제출하는 것을 조건으로 품목허가를 결정했다.
앞으로 식약처는 제조단위 별로 제조사의 제조․시험 결과를 분석하고 직접 검정시험하는 국가출하승인으로 품질을 한번 더 확인할 예정이다.
해당 백신은 미국, 유럽연합, 영국, 스위스, 호주, 캐나다 등 62개국에서 허가 또는 긴급사용승인 등을 받아 5~11세 어린이의 코로나 예방 목적으로 접종에 사용되고 있다.








