코셀루고 급여권 진입…경제성 평가 생략 2번째 사례
약제 급여 적정성 재평가 결과 3개 성분 급여 범위 축소
렉라자(유한양행, 레이저티닙)와 타그리소(아스트라제네카, 오시머티닙)가 내년(2024년) 1월부터 전이성·진행성 비소세포폐암 1차 치료제로 급여가 적용된다.
또한 총상신경섬유종 치료제 코셀루고캡슐(아스트라제네카)도 내년 1월부터 급여권에 진입한다.
보건복지부는 20일 제28차 건강보험정책심의위원회(이하 건정심)을 열고 ▲약제급여 목록 및 급여상한금액표 개정안(신약 등재 및 사용범위 확대 약제 상한금액 조정, 급여적정성 재평가 결과)을 의결했다.
이에 따라 내년 1월부터 국소 진행성·전이성 비소세포폐암 치료제로 렉라자(80mg)와 타그리소(40mg, 80mg)에 대해 1차 치료제로 급여를 적용한다. 유전자 검사 결과 비소세포폐암 관련 유전자변이(EGFR 엑손19 결손 또는 엑손 21(L858R) 치환 변이)가 있는 경우 급여를 인정한다.
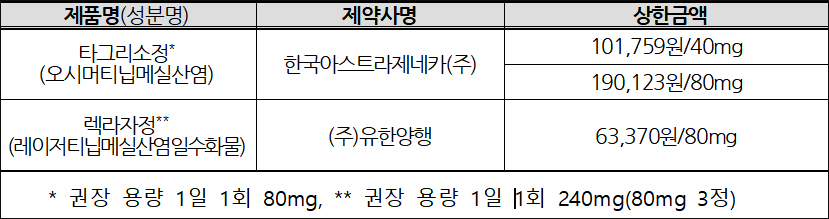
급여 상한금액은 렉라자 80mg이 6만3370원, 타그리소는 40mg이 10만1759원, 80mg이 19만123원이다.
비소세포폐암 환자치료제 렉라자와 타그리소는 이번 급여기준 확대로 치료시작 단계에서부터 급여를 적용할 수 있어 환자의 경제적 부담이 줄어든다.
기존에 국소 진행성 또는 전이성 비소세포폐암 환자 1인당 연간 약 6800만원을 부담했다면 본인부담금 5%를 적용하면 연간 투약비용을 약 340만원까지 절감할 수 있다.
또한 코셀루고 캡슐에 대해서도 내년 1월부터 급여를 적용한다.
해당 약제는 지난 1월부터 중증·희귀질환 신약에 대한 접근성 강화 취지에서 경제성 평가를 생략하고 급여를 적용한 두번째 사례다. 이를 통해 환자 1인당 투약 비용을 약 2억800만원 부담했지만 급여 적용으로 최대 1014만원까지 절감할 수 있게 된다.
코셀루고 캡슐은 수술이 불가능한 총상신경섬유종을 동반한 신경섬유종증 1형인 3세 이상 18세 이하 환자를 대상으로 급여를 적용하며 상한금액은 10mg은 9만5347원, 25mg은 23만464원이다.
급여권 진인에 따라 내년부터 수술이 불가능한 3세 이상 소아·청소년의 총상신경섬유종과 국소 진행성 및 전이성 비소세포폐암 환자들의 경제적 부담이 줄어들게 됐다.
또한 복지부는 레바미피드(위장약), 아세틸엘카르티닌염산염(뇌대사개선약), 록소프로펜나트륨(소염‧진통약), 레보설피리드(위장약), 에피나스틴염산염(알러지약), 히알루론산점안제(안과용약), 리마프로스트알파덱스(순환개선약), 옥시라세탐(뇌대사개선약) 등 8개 성분 급여적정성 재평가를 실시했다.
그 결과 리마프로스트알파덱스, 록소프로펜 나트륨, 에피나스틴염산염 등 3개 성분에 대해 급여범위를 축소했다.
식약처 임상재평가 결과 유효성이 입증되지 않아 이미 급여중지 및 효능·효과가 삭제된 옥시라세탐, 아세틸엘카르니틴염산염 2개 성분 또한 평가 대상에서 빠졌다.
다만, 히알루론산나트륨 점안제의 경우에는 다른 일회용 점안제로의 전환 사용 등을 고려해 일회용 점안제 전반에 대한 급여기준 설정을 함께 고려할 필요가 있다는 평가 결과에 따라 추후 최종 결정할 예정이다.
한편 지난 22년도 재평가 대상 중 식약처 임상재평가 결과 유효성이 입증되지 않은 스트렙토키나제·스트렙토도르나제 성분 22개 품목은 제외됐다.








