심평원, 9차 암질심 결과 공개, 레테브모 급여기준 설정
키프롤리스주+다잘렉스주+덱사메타손 조합 급여기준 확대 불발
한국릴리의 RET 유전자 변이 표적항암제 레테브모(셀퍼카티닙)가 급여권에 한발짝 나가섰다.
건강보험심사평가원은 제9차 암질환심의위원회(이하 암질심) 결과를 2일 공개했다.
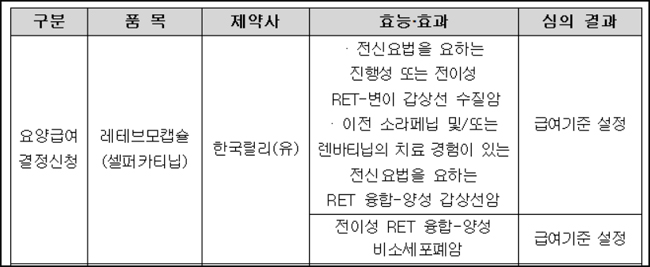
암질심은 릴리가 급여신청한 레테브모캡슐의 갑상선암, 비소세포폐암에 대한 급여기준을 설정했다. 지난 5월 이후 재도전 끝에 급여권 진입에 한 발 다가선 것.
구체적으로 ▲전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암 ▲이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있는 전신요법을 요하는 RET 융합-양성 갑상선암 ▲전이성 RET 융합-양성 비소세포폐암에 대한 급여기준을 만들었다.
레테브모는 우리나라에 들어온 첫 RET 표적항암제로 식품의약품안전처의 신속심사를 통해 허가를 받았다.
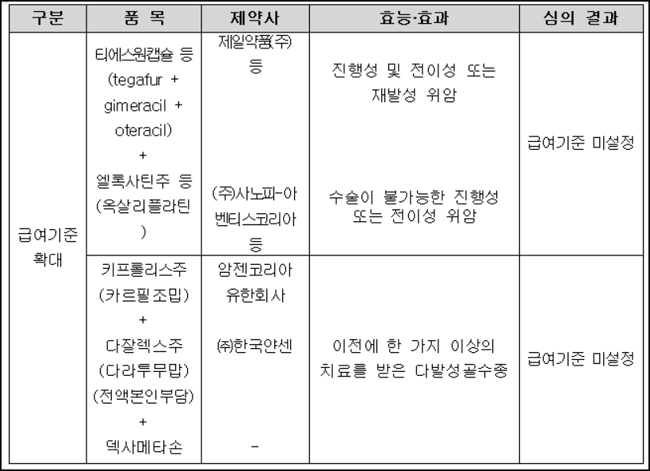
반면, 티에스원캡슐 등(tegafur + gimeracil + oteracil)+엘록사틴주 등(올살리플라틴)은 진행성 및 전이성 또는 재발성 위암, 수술이 불가능한 진행성 또는 전이성 위암으로 급여기준 확대를 노렸지만 불발됐다.
키프롤리스주(카르필조밉)+다잘렉스주(다라투무맙)+덱사메타손 조합도 이전에 한 가지 이상의 치료를 받은 다발성골수종 조합으로 급여기준 확대를 시도했지만 암질심 문턱을 넘지 못했다.
암질심을 통과한 약제는 약제급여평가위원회, 건강보험공단과의 약가 협상 단계를 거친 후 건강보험정책심의위원회에서 급여가 최종 결정된다.








