경북대병원 연구진, 병용 요법의 시너지 효과 기전 밝혀
"면역항암제 사용범위를 확대할 수 있는 치료전략 기대"
글루타민 대사 억제제를 면역항암제와 병용하면 T-림프구에 의한 암세포 사멸을 크게 증가시켜 궁극적으로 종양 크기를 감소케 하는 기전이 규명됐다.

(왼쪽부터) 박근규, 최연경 교수, 변준규 박사, 박미향 박사과정
경북대병원은 내분비대사내과 박근규, 최연경 교수팀(공동 1저자 변준규 박사, 박미향 박사과정)이 암 대사 억제제와 면역항암제의 시너지 효과에 대한 기전을 밝혀냈다고 10일 밝혔다.
박 교수팀 연구결과는 '분자세포(Molecular Cell)' 최신호에 실렸다. 과학기술정보통신부와 한국연구재단에서 추진하는 중견연구자지원사업과 바이오·의료기술개발사업의 지원으로 수행한 연구다.
연구진은 글루타민이 결핍된 종양미세환경에 노출된 암세포는 성장이 둔화되지만 면역회비 단백질로 알려진 PD-L1 발현이 증가해 T-림프구 항종양 면역반응을 회피해 생존할 수 있다는 것을 발견했다.
이에 따라 글루타민 억제제와 항PD-L1 항체를 병용했을 때 T-림프구에 의한 암세포 사멸이 증가하면서 종양 크기도 단독투여 보다 크게 줄었다.
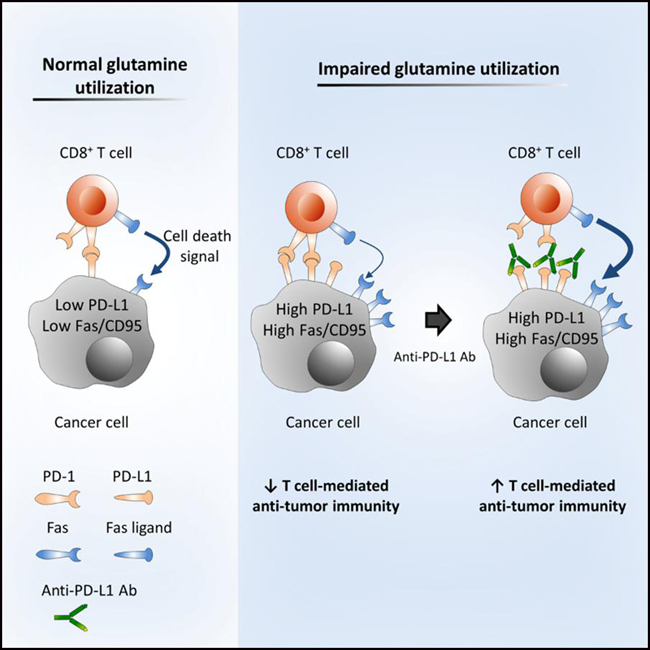
글루타민 대사 억제제와 면역항암제의 병용 효과의 개념도
연구진은 글루타민 대사 억제제가 면역결핍 실험 쥐에서는 뚜렷한 항암효과가 있지만 면역기능이 정상인 쥐에서는 효과가 상쇄된다는 점에 착안했다.
그 결과 글루타민 대사를 억제하거나 글루타민 수송을 차단했을 때 암세포의 PD-L1 발현이 상향조절 돼 T-림프구의 항종양 면역 반응을 저해했다.
또 암세포에서 글루타민 대사를 억제하면 칼슘 펌프(SERCA) 활성 저해와 칼슘 신호전달체계의(calcium/NF-κB) 활성화로 면역회피 단백질인 PD-L1과 세포사멸 유발 단백질(Fas/CD95)이 모두 상향 조절됐다.
박근규 교수는 "면역항암제와 암 대사 억제제 병합치료 요법이 제한된 환자에게 적용되던 면역항암제 사용범위를 확대할 수 있는 치료전략이 될 수 있을 것"이라고 말했다.

박 교수팀 연구결과는 '분자세포(Molecular Cell)' 최신호에 실렸다. 과학기술정보통신부와 한국연구재단에서 추진하는 중견연구자지원사업과 바이오·의료기술개발사업의 지원으로 수행한 연구다.
연구진은 글루타민이 결핍된 종양미세환경에 노출된 암세포는 성장이 둔화되지만 면역회비 단백질로 알려진 PD-L1 발현이 증가해 T-림프구 항종양 면역반응을 회피해 생존할 수 있다는 것을 발견했다.
이에 따라 글루타민 억제제와 항PD-L1 항체를 병용했을 때 T-림프구에 의한 암세포 사멸이 증가하면서 종양 크기도 단독투여 보다 크게 줄었다.

그 결과 글루타민 대사를 억제하거나 글루타민 수송을 차단했을 때 암세포의 PD-L1 발현이 상향조절 돼 T-림프구의 항종양 면역 반응을 저해했다.
또 암세포에서 글루타민 대사를 억제하면 칼슘 펌프(SERCA) 활성 저해와 칼슘 신호전달체계의(calcium/NF-κB) 활성화로 면역회피 단백질인 PD-L1과 세포사멸 유발 단백질(Fas/CD95)이 모두 상향 조절됐다.
박근규 교수는 "면역항암제와 암 대사 억제제 병합치료 요법이 제한된 환자에게 적용되던 면역항암제 사용범위를 확대할 수 있는 치료전략이 될 수 있을 것"이라고 말했다.







