식약처, E2B(R3) 의무 적용키로
정보 관리 자동화·표준화 '이점'
의약품 부작용 정보를 체계적으로 관리하기 위해 식품의약품안전처가 내달 1일부터 의약품 부작용 보고 국제표준서식(E2B(R3))을 적용한 '의약품 부작용 보고 선진화 시스템'을 시범 운영한다.
E2B(R3)는 국제의약품규제조화위원회(ICH)에서 개별 부작용 보고서를 전자적으로 전송하기 위해 도입한 국제 표준서식이다.
E2B(R3) 시스템은 기존 시스템에 비해 인과성 평가를 위한 주요 항목 추가 등 보고항목의 세분화되고 약물이상반응 용어 통일, 시판 후 및 임상시험 단계의 보고체계가 일원화되는 등의 변화가 있다.
이번 시범 사업 실시로 대량의 부작용 정보 관리가 자동화·표준화되고 부작용 정보 분석이 용이해져 유의미한 부작용 정보를 신속·정확하게 탐지 등이 가능하게 돼 의약품 안전관리 강화를 기대할 수 있다.
이번 시범 운영 시스템에 적용하는 주요 내용은 ▲보고 항목에 인과성 평가를 위한 주요 항목을 추가해 230여개로 세분화(종전 88개) ▲약물 이상반응 관련 용어를 국제의약용어(MedDRA)로 통일 ▲시판 후와 임상시험 단계의 부작용 보고체계 일원화 등이다.
국제의약용어(MedDRA)는 ICH에서 발간하며, 전세계적으로 의약품 임상시험 및 시판 후 이상사례 보고 등에 사용하는 표준화된 용어다.
의약품은 정상적으로 투여하거나 사용하더라도 예상하지 못한 부작용이 발생할 수 있으므로 우리나라를 포함한 미국, 유럽, 일본 등에서도 발생한 부작용을 면밀하게 검토·분석해 시판중단, 회수, 사용 시 주의사항 안내 등 환자 안전 조치를 하고 있다.
이번에 개선된 시범 운영 시스템 적용으로 대량의 부작용 정보 관리가 자동화·표준화되고 부작용 정보 분석이 용이해져 유의미한 부작용 정보를 신속·정확하게 탐지하는 것이 가능해진다.
식약처는 그간 의약품 부작용 보고 시스템 도입을 위해 국제표준서식 적용 시스템을 구축(2018년 12월)해 시스템 안정화 기간을 거쳐 이번 시범 운영을 시작하게 됐으며 시범 운영 기간 동안은 기존 보고시스템과 새로운 시스템이 함께 병행해 운영될 예정이다.
식약처는 이번 국제표준서식 적용 시스템 시범 운영으로 의약품 시판 후 안전관리가 보다 강화될 것으로 기대하며, 앞으로도 국민들이 보다 안심하고 의약품을 사용할 수 있도록 더욱 노력하겠다고 밝혔다.
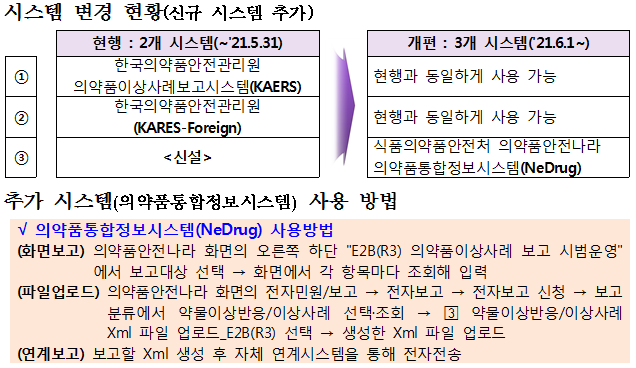
의약품 이상사례 보고 시스템 개편 안내
E2B(R3)는 국제의약품규제조화위원회(ICH)에서 개별 부작용 보고서를 전자적으로 전송하기 위해 도입한 국제 표준서식이다.
E2B(R3) 시스템은 기존 시스템에 비해 인과성 평가를 위한 주요 항목 추가 등 보고항목의 세분화되고 약물이상반응 용어 통일, 시판 후 및 임상시험 단계의 보고체계가 일원화되는 등의 변화가 있다.
이번 시범 사업 실시로 대량의 부작용 정보 관리가 자동화·표준화되고 부작용 정보 분석이 용이해져 유의미한 부작용 정보를 신속·정확하게 탐지 등이 가능하게 돼 의약품 안전관리 강화를 기대할 수 있다.
이번 시범 운영 시스템에 적용하는 주요 내용은 ▲보고 항목에 인과성 평가를 위한 주요 항목을 추가해 230여개로 세분화(종전 88개) ▲약물 이상반응 관련 용어를 국제의약용어(MedDRA)로 통일 ▲시판 후와 임상시험 단계의 부작용 보고체계 일원화 등이다.
국제의약용어(MedDRA)는 ICH에서 발간하며, 전세계적으로 의약품 임상시험 및 시판 후 이상사례 보고 등에 사용하는 표준화된 용어다.
의약품은 정상적으로 투여하거나 사용하더라도 예상하지 못한 부작용이 발생할 수 있으므로 우리나라를 포함한 미국, 유럽, 일본 등에서도 발생한 부작용을 면밀하게 검토·분석해 시판중단, 회수, 사용 시 주의사항 안내 등 환자 안전 조치를 하고 있다.
이번에 개선된 시범 운영 시스템 적용으로 대량의 부작용 정보 관리가 자동화·표준화되고 부작용 정보 분석이 용이해져 유의미한 부작용 정보를 신속·정확하게 탐지하는 것이 가능해진다.
식약처는 그간 의약품 부작용 보고 시스템 도입을 위해 국제표준서식 적용 시스템을 구축(2018년 12월)해 시스템 안정화 기간을 거쳐 이번 시범 운영을 시작하게 됐으며 시범 운영 기간 동안은 기존 보고시스템과 새로운 시스템이 함께 병행해 운영될 예정이다.
식약처는 이번 국제표준서식 적용 시스템 시범 운영으로 의약품 시판 후 안전관리가 보다 강화될 것으로 기대하며, 앞으로도 국민들이 보다 안심하고 의약품을 사용할 수 있도록 더욱 노력하겠다고 밝혔다.








