EGFR 돌연변이 환자 대상 LASER301 연구 전격 발표
아시아인, 뇌전이 환자 효과 뚜렷...관건은 허가와 보험

국산 폐암신약 렉라자(성문명 레이저티닙)가 전 세계 두 번째 3세대 EGFR-TKI(상피세포성장인자수용체-티로신키나제억제제) 1차 치료제라는 타이틀 획득을 눈앞에 두고 있다.
조병철 세브란스병원 종양내과 교수는 3일 유럽임상종양학회 아시아(ESMO-ASIA)에서 전 세계 13개국, 96개 병원이 참여한 LASER301 연구 최종 결과를 발표했다.
그 결과, EGFR 돌연변이 비소세포폐암 환자에게 렉라자로 초치료했을때 1세대 게피티닙 대비 '질병진행 및 사망 위험'을 55% 감소시키는 것으로 나타났다.
이번 연구에서 확인된 레이저티닙 치료군의 무진행생존기간(PFS)은 20.6개월로, 비교군인 게피티닙인 9.7개월보다 두 배 이상 앞서면서 통계적인 유의성을 벌이는데도 성공했다.
특히 무진행생존기간이 20개월을 초과할 수 있다는 새로운 가능성과 기록도 남겼다. 목표했던 1차 종료점이 충족하면서 1차 치료제로서 국내외 적응증 승인 또한 무난할 것으로 예상된다.
아시아인, 유전자 하위분석도 모두 성공
공개된 LASER301 연구는 오시머니티닙의 1차 치료 연구인 FLAURA 연구를 상당 부분 벤치마킹했기 때문에 환자구성 등 연구설정 기준(프로토콜)이 흡사하다.
전체 참여환자는 393명으로, FLAURA 연구보다는 다소 적지만, 비율은 유사하다. 아시아인 참여율은 66%이며(vs 62%), 엑손19 결핍 또는 L858R 치환 유전자 환자군의 비율도 큰 차이가 없다. 평균 연령도 67세로 맞췄다.
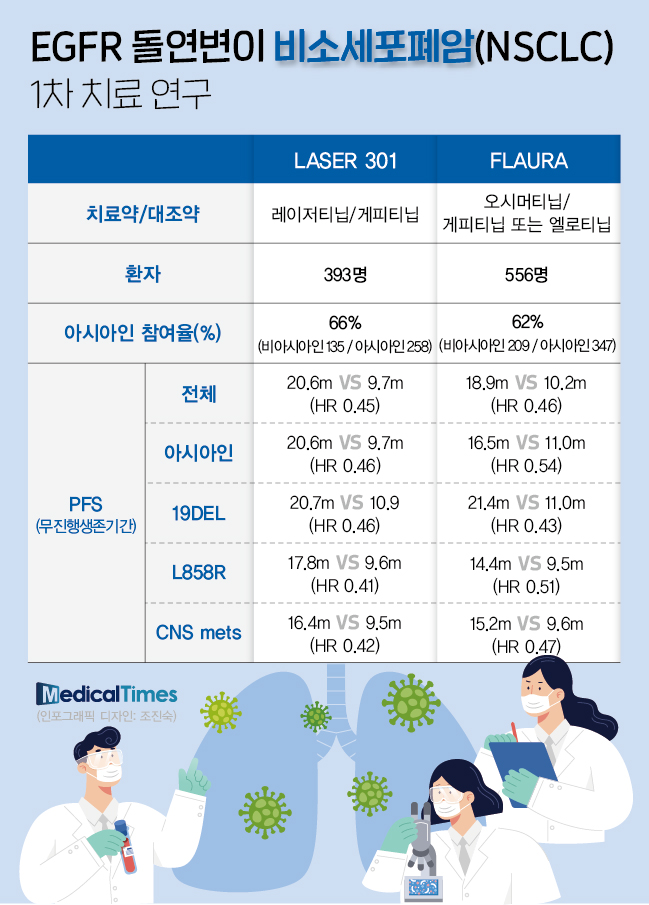
이번 연구에서 관심이 집중됐던 아시아인 하위분석도 모두 공개됐다. 레이저티닙 치료군에서 20.6개월, 게피티닙 치료군 9.7개월로, 전체 환자군 연구 결과치와 동일했으며, 결과적으로 레이저티닙 치료 환자들의 질병 진행 및 사망위험도 54% 더 낮았다.
유전자에 구분에 상관없이 효과도 일관적으로 나타났다.
19DEL 유전자를 가진 환자군(20.7개월 vs 10.9개월)과 L858R 유전자를 가진 환자군(17.8개월 vs 9.6개월)에서 질병 진행 및 사망 위험을 각각 54%와 59% 낮추면서 강력한 3세대 EGFR -TKI 면모를 확인했다.
더불어 뇌전이 환자군 또한 무진행생존기간이 16.4개월과 9.5개월로 차이를 보며, 58%의 상대적 생존율 개선효과를 입증했다.
이로서 레이저티닙은 인종, 유전자 구분, 뇌전이 유무에 상관없이 고른 효과를 보이는 강력한 3세대 EGFR-TKI 1차 치료제로 재탄생할 준비를 마쳤다.
연구에서 확인된 레이저티닙의 부작용은 주로 발진, 설사, 감각 이상, 간수치 증가로 확인됐으나, 대부분 경증으로 대조군인 게피티닙과 유사했다. 문제가 되는 3등급 이상의 부작용은 많지 않았다.
연구를 발표한 조병철 세브란스병원 종양내과 교수는 "강력한 국산 EGFR-TKI 제제가 탄생됐다"며 "효과는 뛰어나고, 부작용은 적은 약이다. 특히 아시아인에서 효과가 매우 뛰어다나"고 총평했다.
특히 "초기 임상에서도 확인된 강력한 억제효과가 최종임상에서도 확인할 수 있었다"라며 "이는 3세대 간에도 차이가 존재한다는 것을 의미한다"며 의미를 부여했다.
주요 한국인 연구자 및 해외연구자 반응
토론자로 참여한 벤 솔로몬 호주 멜버른의대 교수는 "지금까지 발표된 레이저티닙의 효과는 일관적이고, 부작용도 적은 것으로 보인다"면서 "전체 생존율 데이터와 가격을 제외한 모든 체크리스트가 일단 합격점이다. 이번 결과에 따라 아미반타맙과 병용요법인 마리포사(MARIPOSA) 연구 결과가 기대된다"고 평가했다.

로스 수 싱가포르 국림암센터 박사는 "(결과가) 너무 놀랍다. 아주 즐거운 놀라움이었다"라고 표현하면서 "게피티닙에 비해 더 좋았고, 안전성은 유사했다. L858R 환자군에서 워낙 좋은 효과를 보여줬다. 뇌전이 환자 효과도 인상깊었다"고 말했다.
이어 그는 "이번 데이터를 토대로 글로벌 허가도 가능할 것으로 보인다. 오시머티닙 이후 인터네셔널에서 세팅된 3상임상 이었기 때문에 큰 허들을 예상하지는 않는다. 이미 미국에서도 마리포사 1, 2, 크리살리스 1, 2 연구가 진행되기 때문에 그런 면에서 미국 허가 또한 허들은 아니다"라고 강조했다.
벤 교수는 "일차표준치료 옵션으로 올라갈 수 있다. NCCN, ASCO, ESMO 가이드라인에 추가되는 과정에서 허들이 존재하지 않는다. 레이저티닙의 다양한 연구가 진행되고 있는 만큼 앞으로 중요한 3세대 TKI 제제의 백본 약물이 될 것"이라고 말했다.
이상반응에 대한 관심도 컸다.
조 교수는 "감각이상 질문이 나왔지만 중요한 점은 약물을 줄이면 해결이 되고, 결정적으로 약물중단이 없었다는게 포인트"라고 강조했다. 로스 박사는 "오시머티닙도 심장독성이 있다. 각 약물마다 다른 분자구조로 인해 나타나는 특이점이 부작용으로 나타나지만 중대한 약물 중단은 없는 게 중요하다"고 말했다.
크로스오버(유효약물 치환)로 인해 전체 생존율 데이터가 유효하게 나오지 않거나 이로인한 약물 저평가 가능성에 대해서도 큰 이슈가 없을 것으로 전망했다.
로스 교수는 "생존데이터가 임상적으로 유효하게 나오지 않아도 약물 평가가 절하되는 일은 없다. 주요 지표는 무진행생존기간이고, 이후에 어떤 치료냐 어떻게 벨런스를 맞추느냐에 따라 전체 생존율은 약제효과에 영향을 받기 떄문에 이는 크게 의미를 두지 않는다"고 말했다.
현장에서 만난 김열홍 고려안안병원 종양내과 교수는 "두 가지 측면에서 총평해 볼 수 있다. L858R 유전자 환자에게 가장 확신한 효과를 보였고, 뇌전이 환자에게도 강력한 종양억제 효과가 나타났다는 점이 특이점이라고 할 수 있다. 이런 부분에서 좋은 데이터가 만들어졌다는게 중요하다"고 말했다.
한편 조 교수는 급여 추진 이슈와 관련해 "레이저티닙 1차 치료제의 근거가 나온만큼 허가 이후 급여단계에 돌입한다면 같이 같이 리뷰할 가능성이 크다. 또 그렇게 해야한다"고 밝혔다.








