8곳 16개 품목 허가…이레사 특허 만료엔 5개사 '눈독'
로슈의 비소세포폐암 표적항암제 '타쎄바(성분명 : 엘로티닙염산염)'가 이달 30일 특허 만료 된다.
일동제약 등 총 8개 제약사가 제네릭을 출시할 예정인 가운데 12월에는 폐암치료제 이레사의 특허 만료도 예정돼 있어 제네릭 시장이 점차 불붙을 전망이다.
10일 식품의약품안전처에 따르면 타쎄바 제네릭 허가를 받은 제약사는 총 8곳으로 나타났다.
허가를 받은 제약사는 한독테바, 일동제약, 한미약품, 광동제약, 보령제약, CJ헬스케어, 종근당, 한국유나이티드제약이다.
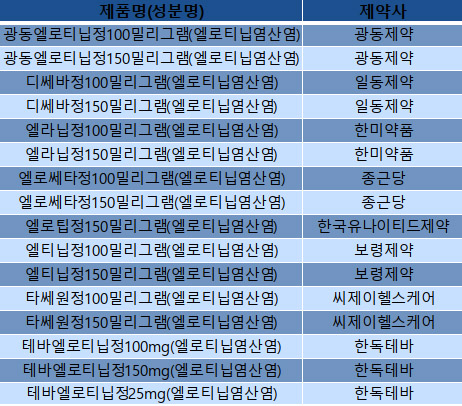
엘로티닙염산염 제네릭 허가 사항
2005년 출시된 오리지널 '타쎄바'는 표적치료제로서 연 처방액 200억원의 대형 품목. 25mg과 100mg, 150mg 라인업을 갖추고 있다.
엘로티닙염산염 단일제의 적응증은 비소세포폐암과 췌장암으로 나뉘는데, 용량에 따라 150mg은 비소세포폐암에, 100mg은 젬시타빈과 병용해 췌장암 치료에 사용된다. 용량에 따라 비소세포폐암 치료나 췌장암 치료 목적이 달라진다는 뜻이다.
먼저 한독테바는 테바엘로티닙정이라는 제품명으로 25mg, 100mg, 150mg 세 가지 용량을 허가 받았다.
일동제약은 디쎄바정, 한미약품은 엘라닙정, 광동제약은 엘로티닙정, 보령제약은 엘티니정, CJ헬스케어는 타쎄원정, 종근당은 엘로쎄타정, 한국유나이티드제약은 엘로팁정으로 각각 허가 목록에 이름을 올렸다.
종근당과 CJ헬스케어, 일동제약, 한미약품 등 다수 제약사는 100mg, 150mg 두 가지 라인업을 갖췄지만 한국유나이티드제약은 150mg으로만 허가를 받았다.
한편 12월 1일 특허가 만료되는 아스트라제네카의 이레사정(성분명 : 게피티니브) 제네릭도 출격 채비를 마쳤다.
제네릭 출시 대기 품목은 종근당의 이레티닙정, 한미약품의 제피티닙정, 광동제약 레피사정, 일동제약 스펙사정, 신풍제약 이레피논정까지 5개다.
일동제약 등 총 8개 제약사가 제네릭을 출시할 예정인 가운데 12월에는 폐암치료제 이레사의 특허 만료도 예정돼 있어 제네릭 시장이 점차 불붙을 전망이다.
10일 식품의약품안전처에 따르면 타쎄바 제네릭 허가를 받은 제약사는 총 8곳으로 나타났다.
허가를 받은 제약사는 한독테바, 일동제약, 한미약품, 광동제약, 보령제약, CJ헬스케어, 종근당, 한국유나이티드제약이다.

엘로티닙염산염 단일제의 적응증은 비소세포폐암과 췌장암으로 나뉘는데, 용량에 따라 150mg은 비소세포폐암에, 100mg은 젬시타빈과 병용해 췌장암 치료에 사용된다. 용량에 따라 비소세포폐암 치료나 췌장암 치료 목적이 달라진다는 뜻이다.
먼저 한독테바는 테바엘로티닙정이라는 제품명으로 25mg, 100mg, 150mg 세 가지 용량을 허가 받았다.
일동제약은 디쎄바정, 한미약품은 엘라닙정, 광동제약은 엘로티닙정, 보령제약은 엘티니정, CJ헬스케어는 타쎄원정, 종근당은 엘로쎄타정, 한국유나이티드제약은 엘로팁정으로 각각 허가 목록에 이름을 올렸다.
종근당과 CJ헬스케어, 일동제약, 한미약품 등 다수 제약사는 100mg, 150mg 두 가지 라인업을 갖췄지만 한국유나이티드제약은 150mg으로만 허가를 받았다.
한편 12월 1일 특허가 만료되는 아스트라제네카의 이레사정(성분명 : 게피티니브) 제네릭도 출격 채비를 마쳤다.
제네릭 출시 대기 품목은 종근당의 이레티닙정, 한미약품의 제피티닙정, 광동제약 레피사정, 일동제약 스펙사정, 신풍제약 이레피논정까지 5개다.








