식약처, 2026년까지 재평가 추진…부적합 시 회수조치
제약사 생동 부담 커져…중소병원 중심 임상기관 역할 커졌다
식품의약품안전처가 경구용 의약품 등을 필두로 대대적은 '동등성 재평가'를 벌인다.
당장 내년부터 정제를 필두로 경구용 의약품의 동등성 재평가를 실시할 예정으로, 국내 제약사를 중심으로 제네릭 의약품을 유지하기 위해 의약품 동등성을 입증해야 하는 부담이 생기게 됐다.

식약처는 14일 오전 의약품 제조‧수입업체의 재평가 업무 담당자를 대상으로 '의약품 재평가 정책설명회'를 온라인으로 개최하고 동등성 재평가 추진 방향을 공개했다.
앞서 식약처는 제네릭 의약품 품질 신뢰성 향상을 위해 생동성 입증 의무를 전 성분‧제형 품목으로 확대 한 바 있다.
이 가운데 식약처는 기허가 의약품에 대해서도 동등성을 입증해야 한다는 필요성이 제기돼 재평가를 실시하고 있다.
이에 따라 2021년에는 산제‧과립제를, 2022년에는 점안제‧점이제‧폐흡입제를 대상으로 동등성 재평가를 벌이고 있다.
여기에 식약처는 향후 4년 간 경구제를 포함해 주사제까지 전 품목에 대한 동등성 재평가를 벌일 것으로 예상된다.
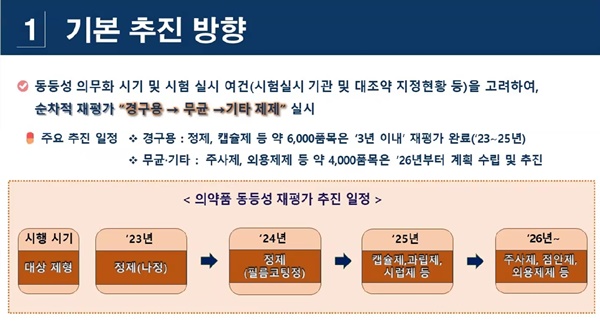
실제로 식약처는 ▲2023년에 경구용 제제 중 정제로 레보드로프로피진 등 130개 ▲2024년 필름코팅정으로 암로디핀 등 420개 성분 ▲2025년 캡슐제, 과립제, 시럽제로 피록시캄 등 286개 성분 ▲2026년 아세트아미노펜 등 984개 성분에 대한 대대적인 생동성 재평가를 벌일 예정인 것으로 나타났다.
앞으로 매 해마다 대상이 된 품목을 보유한 제약사들은 생물학적동등성을 입증해야만 한다.
다만, 생동결과보고서 제출이 어려운 경우, 계획서를 우선 제출하고 계획서에 따른 시험완료 후 결과보고서를 제출하는 형태로 진행한다는 것이 식약처의 방침이다.
따라서 식약처의 생동성 재평가가 진행되는 동안 중소병원 중심으로 이뤄지는 임상시험 건수가 급증할 것으로 예상된다.
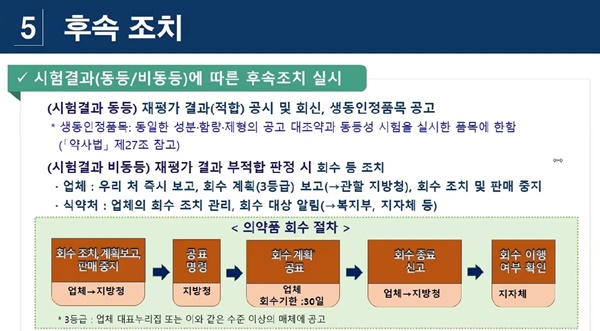
식약처 재평가 결과 적합 판정을 받은 품목을 공고하는 한편, 부적합 판정 시 회수 등의 조치를 진행한다는 계획이다.
식약처 의약품안전평가과 이인선 사무관은 "동등성 의무화 시기 및 시험 실시 여건(시험실시 기관 및 대조약 지정현황 등)을 고려해 순차적으로 경구용, 무균, 기타제제 순으로 실시할 예정"이라며 "2023년부터 2025년까지 정제, 캡슐제 등 경구용 6000품목은 3년 이내 재평가를 완료할 계획"이라고 전했다.








