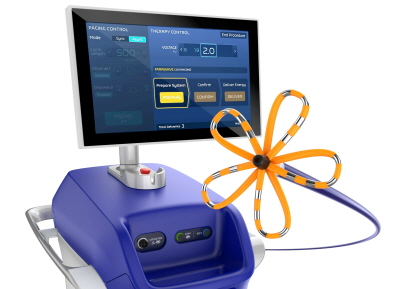
보스톤사이언티픽, 파라펄스 PFA 시스템 국내 허가 획득
메디칼타임즈=이인복 기자보스톤사이언티픽은 파라펄스 PFA 시스템(FARAPULSE Pulsed Field Ablation System)이 펄스장 절제술(Pulsed Field Ablation, PFA)에 사용되는 의료기기 중 최초로 식품의약품안전처 허가를 받았다고 16일 밝혔다. 파라펄스 PFA 시스템은 고온이나 저온을 이용하는 기존의 열 절제술과 달리 펄스장을 통해 문제 조직에 선택적으로 작용해 식도와 같은 주변 구조에 손상을 피할 수 있어 심방세동 치료의 새로운 대안으로 빠르게 성장하고 있다.파라펄스 PFA 시스템은 파라웨이브 카테터(FARAWAVE PFA Catheter), 파라스타 제너레이터(FARASTAR Pulsed Field Ablation Generator), 파라드라이브 시스(FARADRIVE Steerable Sheath)로 구성된다. 특히 꽃과 바구니 모양을 특징으로 하는 파라웨이브 카테터는 개별 환자의 다양한 해부학적 구조에 맞게 장치를 조정할 수 있어 사용 편의성을 높이고 시술자에 따른 차이를 줄일 수 있도록 했다.파라펄스 PFA 시스템은 다양한 임상 근거와 실제 임상 결과를 통해 효과성과 안전성을 확인한 제품이다.실제로 파라펄스 PFA 시스템을 사용한 펄스장 절제술과 열 절제술의 효능과 안전성을 직접 비교한 무작위 임상 시험인 어드벤트(ADVENT) 연구 결과 펄스장 절제술이 기존의 열 절제술만큼 안전하고 효과적일 뿐만 아니라 절제술 소요 시간을 줄이고 시술자의 학습 곡선(Learning Curve)도 개선한 것으로 나타났다. 또한 파라펄스 PFA 시스템을 사용한 1만 7천 명 이상의 환자의 실제 임상 결과를 분석한 메니페스트-17K(MANIFEST-17K) 레지스트리에서도 영구적인 신경마비, 폐정맥 협착, 식도 손상 등이 보고되지 않아 파라펄스 PFA 시스템의 안전성을 다시 한번 확인했다.정애리 보스톤사이언티픽 한국 총괄 대표는 "현재까지 전 세계적으로 12만 5천 명 이상의 환자에 사용되면서 임상 근거가 다양하게 축적된 파라펄스 PFA 시스템을 한국에도 가장 먼저 선보일 수 있게 되어 기쁘다"며 "PFA가 국내 임상 현장에도 빠르게 상용화되도록 힘쓰며 국내 시장을 선도하도록 노력할 것"이라고 말했다. 한편, 파라펄스 PFA 시스템은 2019년 FDA로부터 혁신의료기기(Breakthrough Device Designation)로 지정되고 2021년 유럽 통합규격인증(CE)을 받았으며 현재까지 미국, 일본, 유럽 등 65개국 이상에서 허가를 받았다. 또한 국내에서는 보건복지부 신의료기술 평가 결과 고시 이후 본격적으로 출시될 예정이다.