'포말리스트' 퍼스트제네릭 차지한 보령…선점 효과 볼까
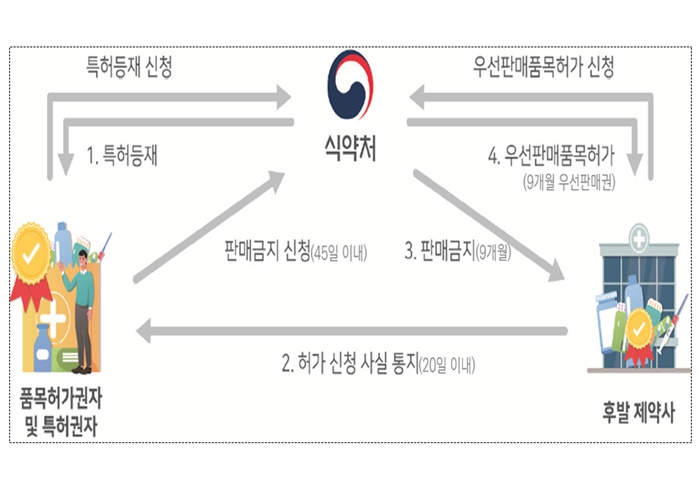
메디칼타임즈=허성규 기자보령이 다발골수종 치료제 '포말리스트(포말리도마이드)'의 퍼스트 제네릭을 허가 받으면서 복제약 시장 경쟁에서 한발 앞서 나가게 됐다. 다만 당연히 따라올 것으로 기대했던 우판권 획득에는 실패하면서 광동제약 등 후발주자의 진입 전에 빠르게 점유율을 확대해야 할 것이라는 전망이 나오고 있다. 보령이 포말리스트의 퍼스트제네릭의 허가를 획득하며 제네릭 시장 경쟁에서 앞서나가게 됐다.12일 업계 및 식약처에 따르면 보령은 최근 포말리도마이드 성분의 포말리킨캡슐 4개 용량을 허가 받았다.해당 성분 제제의 오리지널 품목은 세엘진의 다발골수종 치료제인 '포말리스트'다.포말리스트는 아이큐비아 기준 지난해 매출 약 228억원 규모를 나타내는 품목으로 국내 제약사 중에서는 광동제약과 보령 두곳이 제네릭 허가를 노리고 있었다.이를 위해 오는 2030년 만료되는 포말리스트의 제제 특허에 대해서 광동제약과 보령은 도전장을 내밀었고 지난 2021년 두곳 모두 회피에 성공했다.하지만 두 제약사 모두 허가를 진행하지 않았다. 이후 보령이 올해 초 다시 동일한 특허에 소극적권리범위 확인 심판을 청구하며, 재도전에 나섰다.결국 보령은 지난 6월 두 번째 특허 회피에도 성공했고, 최근 퍼스트제네릭까지 허가 받으며 한발 앞서 나가게 됐다.하지만 보령의 퍼스트제네릭 차지에도 우선판매품목허가(이하 우판권)을 획득하지 못한 것으로 파악된다.우판권을 획득할 경우 약 9개월간의 제네릭 시장 독점권을 얻게 되지만 보령은 이를 얻지 못한 것.이에 퍼스트제네릭으로 시장 선점 효과를 극대화하기 위해서는 빠른 출시가 필요한 상황이 됐다.다만 후발주자 경쟁에는 변수가 남아있어 이후 구도는 지켜봐야할 전망이다.앞서 보령이 재도전에 나선 것처럼 광동제약의 역시 지난 특허 회피 당시와는 다른 개발 방식을 선택할 가능성이 남아있기 때문이다.실제로 광동제약의 허가 신청이 아직까지도 이뤄지지 않은 것으로 알려져 있다.이에따라 광동제약이 후발주자로 어떻게 진입할지는 물론 보령이 어떤 전략으로 시장 선점 효과를 노릴지에 관심이 주목된다.